Медучреждения, в которые можно обратиться Общее описание
Очаговая травма головного мозга (ушиб головного мозга легкой степени) (S06.3) — это черепно-мозговая травма с локальным поражением тканей головного мозга, характеризующаяся наличием очага некроза нервной ткани.
Распространенность: 130 на 100 тысяч человек. Чаще встречается у мужчин (60%).
Клиническая картина
Симптомы появляются внезапно в результате травмы головы. Длительность потери сознания — до 20 минут. Одновременно с нарушением сознания появляются симптомы болезни (головная боль, головокружение, тошнота, иногда рвота, слабость/онемение в одной половине тела) в течение нескольких часов, дней. После восстановления сознания спутанность остается в течение суток. Характерна потеря памяти на момент травмы. Симптомы заболевания проходят в течение 2–3 недель.
При неврологическом осмотре пациента выявляют нарушение сознания (90%), общемозговой синдром (90%), менингеальные симптомы (40%), кон-/ретро-/антероградную амнезию (75%), содружественные/несодружественные плавающие движения глазных яблок (30%), легкую анизокорию, спонтанный нистагм (50%), контралатеральный гемипарез/гемигипестезию (20%), повышение мышечного тонуса (30%), вегетативные реакции (тахи-/брадикардию, артериальную гипертензию) (40%).
Диагностика очаговой травмы головного мозга
- Измерение артериального давления.
- Люмбальная пункция (повышенное ликворное давление до 200 мм водяного столба).
- Рентгенография черепа (линейный перелом костей свода черепа).
- Компьютерная и магнитно-резонансная томография головного мозга (наличие гиподенсивного очага, соответствующего локальному отеку; линейные переломы костей свода черепа).
Дифференциальный диагноз: другие черепно-мозговые травмы.
Лечение очаговой травмы головного мозга
Лечение включает госпитализацию, постельный режим в течение 7–10 суток, анальгетики, ноотропы, сосудистые препараты, диуретики. Назначается только после подтверждения диагноза врачом-специалистом.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Трамадол (анальгезирующее средство). Режим дозирования: в/в, в/м, п/к в разовой дозе 50-100 мг, возможно повторное введение препарата через 4-6 ч. Максимальная суточная доза — 400 мг.
- Пирацетам (ноотропный препарат). Режим дозирования: внутрь во время приема пищи или натощак, запивая жидкостью. Начальная доза составляет 800 мг в 3 приема, при улучшении состояния разовую дозу постепенно снижают до 400 мг. Суточная доза 30-160 мг/кг, кратность приема — 2 раза/сут., при необходимости 3-4 раза/сут. Последнюю разовую дозу следует принимать не позднее 17 ч. Курс лечения продолжают от 2-3 нед. до 2-6 мес. При необходимости курс лечения повторяют.
- Диакарб (диуретик из группы ингибиторов карбоангидразы). Режим дозирования: взрослым назначают по 250-500 мг однократно утром в течение 3 дней, на 4-й день — перерыв.
- Кавинтон (препарат, улучшающий мозговое кровообращение). Режим дозирования: внутривенно 20-25 мг в 500 мл инфузионного раствора. В течение 2-3 дней дозу можно увеличить не более чем до 1 мг/кг/сутки. Средняя продолжительность курса 10-14 дней. По окончании курса внутривенной терапии рекомендуется продолжить лечение таблетками Кавинтон по 2 таблетки 3 раза в сутки.
| • | Ведущие специалисты и учреждения по лечению данного заболевания в России: |
| директор НИИ нейрохирургии им. Бурденко Н.Н. Коновалов А.Н. | |
| • | Ведущие специалисты и учреждения по лечению данного заболевания в мире: |
| Professor Duke Samson, USA. |
Заболеваемость (на 100 000 человек)
| Мужчины | Женщины | |||||||||||||
| Возраст, лет |
0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + | 0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + |
| Кол-во заболевших |
0 | 0 | 1.3 | 1.5 | 1.5 | 1.5 | 0.5 | 0 | 0 | 1.3 | 1.5 | 1.5 | 1.5 | 0.5 |
Что нужно пройти при подозрении на заболевание
- ЭлектроэнцефалографияПри легкой травме головного мозга изменения на ЭЭГ могут отсутствовать либо регистрируются лишь незначительные нарушения показателей мозговых потенциалов в виде усиления частых колебаний и неравномерности α-ритма. При этом возможно наличие межполушарной асимметрии, а также электрографических признаков поражения мозгового ствола.
Симптомы
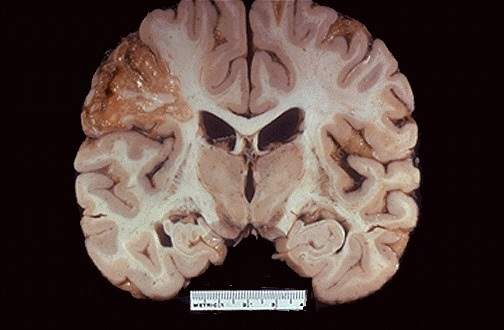
Выделяют несколько важных органов, без работы которых мы не сможем жить. Один из них – головной мозг. При диффузных или очаговых поражениях головного мозга страдает слаженная работа всего организма.
Локальное (очаговое) поражение – это местное повреждение структур мозгового вещества, проявляющееся расстройством определенных функций. Другими словами, в сером или белом веществе возникает патологический очаг (образование), которому сопутствует неврологическая симптоматика. Для большей наглядности стоит перечислить все причины по частоте встречаемости.
Сосудистые нарушения
Это одна из самых обширных групп, так как болезни сердечно-сосудистой системы по статистике занимают первое место в мире. Сюда можно отнести острые нарушения мозгового кровообращения (ОНМК). Именно инсульты играют ведущую роль в появлении очаговых изменений в головном мозге сосудистого генеза.
Под влиянием кровоизлияния или ишемии в сером веществе формируется патологический очаг, приводящий к возникновению неврологических симптомов. Клиническая картина напрямую будет зависеть от обширности очага, его локализации, фактора, вызвавшего нарушение кровообращения.
Полезно узнать, что такое глиозные изменения головного мозга: лечение, диагностика, профилактика.
Все про лейкоареоз головного мозга: степени, симптомы.
Новообразования
Не менее важная группа причин органического поражения мозга. Занимает второе место по частоте встречаемости. Все новообразования можно разделить на доброкачественные или злокачественные.
Иногда доброкачественные опухоли могут никак себя не проявлять, но по мере роста они сдавливают соседние нервные структуры, повышают внутричерепное давление, дают о себе знать различными неврологическими расстройствами. Характерно, что в 50% случаев они полностью излечиваются хирургически.
Раковые очаговые изменения вещества мозга могут быть единичными или множественными, что значительно ухудшает прогноз. Также опухоль бывает первичной или метастатической (занесенной из другого пораженного органа). Лечение таких очаговых поражений является крайне сложным, а в большинстве случаев безуспешным.
Травмы головного мозга
Чтобы в сером или белом веществе возникли участки повреждения, травмирующий фактор должен быть довольно сильным. В эту группу можно отнести тяжёлые ушибы головы, сдавление, проникающие ранения. После таких травм появляются очаги демиелинизации, ишемии, некроза, кровоизлияния. Неврологические симптомы зависят от локализации повреждённой структуры.
Дегенеративные изменения
Появляются к старости в результате атеросклероза, обменных нарушений, кислородного голодания нервной ткани, обезвоживания, органических заболеваний (болезнь Альцгеймера, Пика, Паркинсона, рассеянный склероз). Связаны такие изменения с физиологическими возрастными процессами, происходящими во всех органах.
Инфекции
Причиной повреждения могут стать вирусы, бактерии, простейшие, паразиты, грибы. Чаще инфекционное воспаление диффузно затрагивает оболочки или вещество, но возможно появление участков поражения (например, эхинококкоз или туберкулёма).
Интоксикации
В практике врачей-неврологов часто встречаются алкогольные, наркотические, лекарственные, химические (соли металлов) очаговые изменения вещества головного мозга под воздействием соответствующих факторов. Следствием подобных отравлений являются множественные участки повреждения в нервной ткани.
Перинатальные поражения мозга у детей
Это обширная область очаговых повреждений головного мозга плода и новорождённого ребёнка, лечением которых занимаются детские неврологи.
Виды очаговых изменений вещества мозга
К очаговым образованиям относят:
- ишемические инсульты, кровоизлияния;
- опухоли (шваннома, глиома, нейробластома, гемангиома), метастазы;
- участки некроза, сдавливания, размозжения нервной ткани;
- очаги склероза и демиелинизации;
- туберкулёма, паразитарные кисты, абсцесс.
Общая и очаговая неврологическая симптоматика
Условно все клинические симптомы можно разделить: общие, очаговые неврологические, а также психические. Общая симптоматика предполагает появление слабости, сонливости, повышения температуры тела, озноба, снижения аппетита, головных болей, головокружения. Опытный врач невролог сможет с 90% точностью определить участок повреждения в головном мозге на основании жалоб и клинических симптомов пациента.
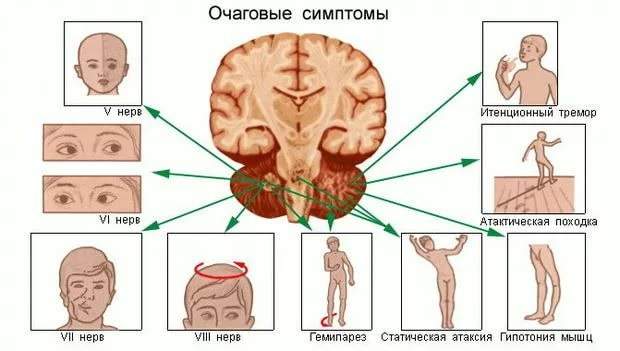
Если очаг расположен в коре лобной доли, то страдает речь, её восприятие, повышается тонус некоторых мышц, возникает расстройство движения глаз, головы, конечностей, теряется равновесие при ходьбе.
При поражении теменной доли нарушается способность читать, писать, считать, изменяется или утрачивается тактильная чувствительность. Больной не может правильно в пространстве определить положение своих конечностей.
Если возникают нарушения слуха, глухота, слуховые галлюцинации, потеря памяти, эпилептические припадки, то можно предположить, что патологический очаг находится в височной доле.
Различные нарушения зрения (изменения цвето- и светоощущения, зрительная иллюзия, полная слепота) говорят в пользу повреждения затылочной доли.
Что такое болезнь Бинсвангера: признаки, лечение и прогноз.
Полезно прочитать, как проявляется микроангиопатия головного мозга: причины, симптомы, последствия.
Что такое мультиформная глиобластома головного мозга: причины, проявления, лечение, прогноз.
Очаги в мозжечке сказываются на равновесии и походке. На самом деле в практике встречается гораздо больше очаговой неврологической симптоматики: парезы, параличи, нарушение чувствительности конечностей, обмороки, тремор. Даже при единичных очаговых изменениях в веществе головного мозга могут возникнуть нарушения дыхания, судороги, кома.
Психические симптомы сопровождают неврологические симптомы, но иногда встречаются сами по себе. К нарушениям психики можно отнести дурашливость, депрессию, раздражительность, нарушение сна, тревожное расстройство, беспокойство, приступы паники или агрессии.
Диагностика очаговых поражений головного мозга
Современные возможности медицины позволяют с высокой точностью диагностировать очаговые поражения головного мозга, их количество, локализацию, размеры. Наиболее информативными обследованиями считаются МРТ, КТ (иногда с контрастом). Также диагностике помогает имеющаяся неврологическая симптоматика.
Лечение очаговых образований
Терапия будет напрямую зависеть от причины появления очагов в головном мозге. При инфекции применяют антибиотики, при травме – диуретики, противоотечные, противосудорожные препараты. Если заболевание вызвано нарушением кровообращения, то для лечения используют сосудистые лекарства, ноотропы, антикоагулянты. Терапия злокачественных опухолей подразумевает облучение, введение цитостатиков, гормонов, оперативное вмешательство.
На заметку! Лечением очаговых образований занимается врач-нейрохирург вместе с неврологом и психиатром.
Прогноз
Сложно сказать, какими будут прогноз и последствия при выявлении очагов в мозге. Этот вопрос решается в индивидуальном порядке и зависит от множества факторов:
- возраста пациента;
- размеров, локализации очага;
- причины, вызвавшей их появление;
- индивидуальных особенностей больного человека.
Заключение
Подводя итоги, можно сказать с уверенностью: при обнаружении клинических признаков очагового поражения мозга стоит незамедлительно обратиться к врачу, а также пройти обследование. Ранняя диагностика является залогом успешного лечения.
(
оценок, среднее:
из 5)
.
К ушибам головного мозга относят возникшие в результате травмы очаговые макроструктурные повреждения его вещества.
КЛАССИФИКАЦИЯ
По принятой в России единой клинической классификации ЧМТ очаговые ушибы мозга разделяют на три степени по тяжести: 1) легкие, 2) среднетяжелые и 3) тяжелые.
Ушиб головного мозга легкой степени
Патоморфологичееки ушиб легкой степени характеризуется сгруппированными точечными кровоизлияниями, ограниченными разрывами мелких пиальных сосудов и участками локального отека вещества мозга.
Ушиб мозга легкой степени встречается у 10— 15% пострадавших с ЧМТ. Характеризуется кратковременным выключением сознания после травмы (несколько секунд — несколько минут). По его восстановлении типичны жалобы на головную боль, головокружение, тошноту и др. Наблюдается ретро-, кон-, антероградная амнезия. Рвота, иногда повторная. Жизненно важные функции обычно без выраженных нарушений. Могут встречаться умеренные брадикардия или тахикардия, иногда — артериальная гипертензия. Дыхание, а также температура тела без существенных отклонений. Неврологическая симптоматика обычно мягкая (клонический нистагм, легкая анизокория, признаки пирамидной недостаточности, менингеальные симптомы); регрессирует в течение 2—3 недель.
При ушибе мозга легкой степени возможны переломы костей свода черепа и незначительное субарахноидальное кровоизлияние.
КТ в половине наблюдений выявляет в мозговом веществе ограниченную зону пониженной плотности (см. рис. 10—5, см. т. I, рис. 19—2А), близкую по томоденситометрическим показателям к отеку головного мозга (от 18 до 28 Н). При этом возможны, как показали и патоло го анатомические исследования, мелкие кровоизлияния. В другой половине наблюдений ушиб мозга легкой степени не сопровождается очевидными изменениями КТ картины, что может быть связано и с ограничениями используемой аппаратуры. Отек мозга при ушибе легкой степени бывает не только локальным, но и более распространенным. Он может проявляться умеренным объемным эффектом, вызывая сужение ликворных пространств. Изменения, обнаруживаясь в первые часы после травмы, обычно достигают максимума на третьи сутки и исчезают через 2 недели, не оставляя гнездных следов. Локальный отек при ушибе легкой степени может быть также изоплотным, и тогда диагноз основывается на объемном эффекте, а также результатах динамического КТ исследования.
МРТ (при использовании полей высокого напряжения) при ушибах мозга легкой степени выявляет ограниченные участки изменения сигналов, соответствующие локальному отеку.
Ушиб головного мозга средней степени
Патоморфологичееки ушиб мозга средней степени характеризуется мелкоочаговыми кровоизлияниями, очагами геморрагического размягчения или геморрагического пропитывания мозговой ткани при сохранности конфигурации борозд и извилин.
Среднетяжелый ушиб мозга встречается у 8—10% пострадавших с ЧМТ. Характеризуется выключением сознания после травмы до нескольких десятков минут — нескольких часов. Выражены ретро-, кон- и антероградная амнезия. Головная боль, часто сильная, может наблюдаться рвота, порой многократная. Встречаются нарушения психики. Возможны преходящие расстройства жизненно важных функций: брадикардия или тахикардия, повышение артериального давления; тахипноэ без нарушения ритма дыхания и проходимости трахеобронхиального дерева; субфебрилитет. Часто выражены оболочечные признаки. Могут улавливаться отдельные стволовые симптомы, чаще всего нистагм. Отчетливо проявляется очаговая симптоматика (определяемая локализацией ушиба мозга): зрачковые и глазодвигательные нарушения, парезы конечностей, расстройства чувствительности, речи и т. д. Эти гнездные знаки постепенно (в течение 3—5 нед) сглаживаются, но могут держаться и длительно.
При ушибе головного мозга средней степени нередко наблюдаются переломы костей свода и основания черепа, а также значительное субарахноидальное кровоизлияние.
КТ в большинстве наблюдений выявляет очаговые изменения в виде некомпактно расположенных в зоне пониженной плотности высокоплотных включений (см. рис. 10—1, 9—11, 9—14), либо — умеренного гомогенного повышения плотности на небольшой площади (см. рис. 9—1, см. т. I, рис. 19— 5). Как показывают данные операций и вскрытий, указанные КТ-находки соответствуют небольшим кровоизлияниям в зоне ушиба или умеренному геморрагическому пропитыванию мозговой ткани без грубой ее деструкции. Динамическая КТ обнаруживает, что эти изменения подвергаются обратному развитию в процессе лечения. В части наблюдений при клинике ушиба мозга средней степени КТ выявляет очаги пониженной плотности — локальный отек, либо травматический субстрат убедительно не визуализируется.
Ушибы мозга средней степени при МРТ выявляются в виде очаговых изменений гетерогенной или гомогенной структуры, что определяется особенностями кровоизлияний в зоне ушиба и их давностью, и отражают ситуацию геморрагического пропитывания мозговой ткани без грубой ее деструкции (см. рис. 9—10, 9—15, 9—16).
Ушиб головного мозга тяжелой степени
Патоморфологически ушиб мозга тяжелой степени характеризуется участками травматического разрушения мозговой ткани с образованием детрита, множественными геморрагиями (жидкая кровь и ее свертки) при утрате конфигурации борозд и извилин и разрыве связей с мягкими мозговыми оболочками.
Тяжелый ушиб мозга встречается у 5—7% пострадавших с ЧМТ. Характеризуется выключением сознания после травмвт продолжителвностью от нескольких часов до несколвких недель. Часто выражено двигателвнос возбуждение. Наблюдаются тяжелые угрожающие нарушения жизненно важных функций: брадикардия или тахикардия; артериальная гипертензия; нарушения частоты и ритма дыхания, которые могут сопровождаться нарушениями проходимости верхних дыхательных путей. Выражена гипертермия. Часто доминирует первично-стволовая неврологическая симптоматика (плавающие движения глазных яблок, парезы взора, тонический множественный нистагм, нарушения глотания, двусторонний мидриаз или миоз, дивергенция глаз по горизонтальной или вертикальной оси, меняющийся мышечный тонус, децеребрационная ригидность, угнетение или ирритация сухожильных рефлексов, рефлексов со слизистых и кожных покровов, двусторонние патологические стопные рефлексы и др.), которая в первые часы и дни после травмы затушевывает очаговые полушарные симптомы. Могут выявляться парезы конечностей (вплоть до параличей), подкорковые нарушения мышечного тонуса, рефлексы орального автоматизма и т.д. Иногда отмечаются генерализованные или фокальные судорожные припадки. Общемозговые и в особенности очаговые симптомы регрессируют медленно; часты грубые остаточные явления, прежде всего со стороны двигательной и психической сфер.
Ушиб головного мозга тяжелой степени обычно сопровождается переломами свода и основания черепа, а также массивным субарахноидальным кровоизлиянием.
При ушибах мозга тяжелой степени КТ часто выявляет очаговые изменения мозга в виде зоны неоднородного повышения плотности (см. рис. 9—12, 9—13). При локальной томоденситометрии в них определяется чередование участков, имеющих повышенную от 64 до 76 Н (плотность свежих свертков крови) и пониженную плотность от 18 до 28 Н (плотность отечной и/или размозженной ткани мозга). Как показывают данные операции и вскрытий, КТ отражает такую ситуацию в зоне ушиба, при которой объем мозгового детрита значительно превышает количество излившейся крови. В наиболее тяжелых случаях деструкция вещества мозга распространяется в глубину, достигая подкорковых ядер и желудочковой системы.
Почти в половине наблюдений ушиба мозга тяжелой степени КТ выявляет значительные по размерам очаги интенсивного гомогенного повышения плотности в пределах от 65 до 76 Н (см. рис. 25; см. т. I, рис. 2—4). Как показывают данные операций и вскрытий, томоденситометрические признаки таких ушибов указывают на наличие в зоне повреждения мозга смеси жидкой крови и ее свертков с детритом мозга, количество которого начинает уступать количеству излившейся крови. Для очагов размозжения характерна выраженность перифокального отека с формированием гиподенсивной дорожки к ближайшему отделу бокового желудочка, через которую осуществляется сброс жидкости с продуктами распада мозговой ткани и крови (см. рис. 9-12, 9-16).
Тяжелые ушибы мозга четко визуализирует МРТ, выявляя зоны гетерогенного изменения интенсивности сигналов (см. рис. 9—3, 9—12, см. т. I, рис. 20-13).
МЕХАНИЗМЫ ОБРАЗОВАНИЯ И ПАТОМОРФОЛОГИЯ
Первичные травматические деструкции и некрозы вешества мозга являются результатом воздействия на него повреждающей механической энергии или самого травмирующего агента в момент ЧМТ. Ушибы мозга развиваются в зоне удара или противо-удара, в области вдавленного перелома или внедрения костных отломков, вокруг раневого канала и т. д. (рис. 9-1, 9-2, 9-3, см. рис. 9—13, 9-14).
При микроскопическом исследовании первичные контузионные повреждения представляют собой очаги деструкции, некроза, геморрагического размягчения или геморрагического пропитывания вещества мозга. В них выделить: а) зону непосредственного тканевого разрушения: б) зону необратимых изменений; в) зону обратимых изменений.
Вторичные травматические (посттравматические) некрозы развиваются спустя некоторое время после травмы. Причиной их возникновения могут быть нарушения кровообращения, ликвородинамики,
а также воспалительные процессы. На свежих срезах нефиксированного мозга вторичные некрозы выделяются в виде ишемических и геморрагических очагов размягчения в белом веществе, являющихся как бы продолжением очага первичного травматического некроза
Одной из причин возникновения вторичных периконтузионных некрозов, является снижение мозгового кровотока в этой зоне. Так, Y. Katayama с соавт., показали, что в центральной части очага контузии снижение кровотока до уровня ишемии наступает тотчас после нанесения травмы. В периконтузионной зоне кровоток вначале временно усиливается, а затем в течение 3 часов после травмы уменьшается до уровня ишемии. Через 6 часов после травмы тромбоз сосудов обнаруживается уже не только в очаге контузии, но и в периконтузионной зоне, что, в конечном счете, ведет к развитию вторичных некрозов.
Изучением морфологии ушибов мозга занимались как отечественные, так и зарубежные патологи. Первый пик исследований пришелся на период после Второй мировой войны.
Морфологическая характеристика очага ушиба мозга, в общем, не имеет особых отличий, зависящих от возраста пострадавшего. Исключение составляют только случаи тяжелой ЧМТ у новорожденных и в раннем детском возрасте. В этой возрастной группе довольно часты разрывы белого вещества, особенно в лобной и височной долях.
Под ушибом мозга понимают очаг первичного повреждения (некроза) вещества мозга в сочетании с кровоизлиянием в эту зону. В очаге ушиба может преобладать кровоизлияние, в редких случаях первичный некроз может не сопровождаться кровоизлиянием.
Наиболее типична локализация ушибов мозга при ЧМТ на выступающих поверхностях мозга, на вершине извилин, вплотную прилегающих к внутренней поверхности костей черепа. Это — полюса и орбитальные поверхности лобных долей (см. рис. 9—1, 9—2), латеральная и нижняя поверхности височных долей и кора над и под сильвиеиой щелью (см. рис. 9—17), также характерна локализация ушибов мозга в конвекситальной коре (см. рис. 9—14). Ушибы теменной и затылочной долей и мозжечка, встречаются при переломах костей черепа (см. рис. 9—18, 9—19). На основании мозга, в области базальных субарахноидальных цистерн, ушибы мозга практически не встречаются. Значительно реже наблюдаются ушибы ствола мозга (см. рис. 9-20, 9-21).
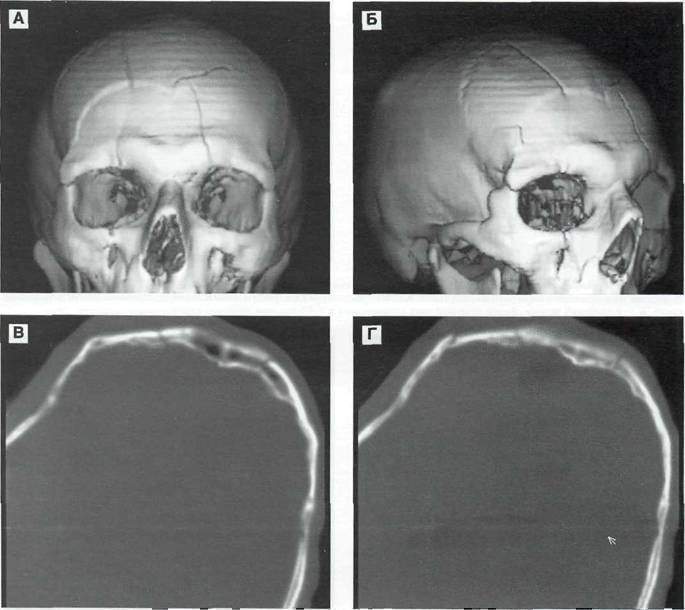
Рис. 9—1. Ударный механизм формирования очагов контузии при вдавленном переломе лобной кости с растрескиванием. КТ. А, Б — трехмерная реконструкция костей свода черепа и лицевого скелета. В, Г — костный режим. Д — тканевой режим. Геморрагические ушибы в передних отделов лобных долей.
Ушиб мозга возникает как в результате непосредственного воздействия механической энергии в месте удара, так и в результате противоудара о противоположные стенки черепа или большой серповидный отросток, мозжечковый намет. Ушиб мозга может возникнуть как при переломе костей, так и неповрежденных костях черепа.
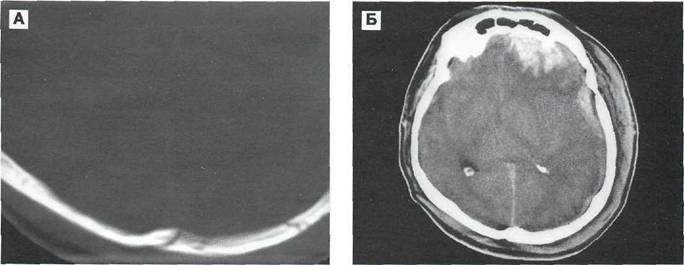
В зависимости от механизма травмы ушибы мозга принято разделять на несколько подтипов: 1) ушиб мозга на месте перелома костей. Локализация очагов ушиба в таких случаях совпадает с участком перелома костей и может наблюдаться как при открытой, так и закрытой ЧМТ;
Рис. 9—2. Противоударный механизм формирования контузионного очага в левой лобной доле в сочетании с субдуральной гематомой при переломе чешуи затылочной кости. К.Т. А — костный режим. Видны множественные переломы чешуи затылочной кости. Б — в тканевый режим. Виден крупный очаг размозжения и субдуральная гематома слева.
Рис. 9—3. Очаги размозжения: ударный в проекции теменной доли слева и противоударный — лобно-базальной локализации справа. МРТ в режиме Т1. А — аксиальная томограмма, Б — фронтальная томограмма.
2) ушиб мозга на месте приложения силы удара (Coup contusion). Ушиб мозга возникает в случаях, когда сила внезапного и локального вдавления костей черепа превышает толерантность прилежащих отделов мозговых оболочек и вещества мозга.
Разрыв сосудов мягкой мозговой оболочки обычно является результатом сильного натяжения, которое возникает при быстром возвращении к своей нормальной конфигурации локально сдавленного эластичного участка кости. При превышении силы удара эластичности костей происходит перелом костей черепа и ушиб прилежащего участка мозга;
3) ушиб мозга, расположенный в противоположной стороне от места приложения удара(contrecoup contusion). Классическим приме
ром является ушиб полюсов лобных долей при падении на затылок;
4) ушибы мозга вследствие удара о край мозжечкового намета и большого затылочного отверстия, при вклинении в момент травмы.
Повреждения обнаруживаются на парагиппокамповых извилинах и миндаликах мозжечка. Чаще наблюдаются при огнестрельных ранениях, но могут встретиться и при закрытой черепно-мозговой травме;
5) скользящий или парасагиттальный ушиб мозга или ушиб Lindcnbcrg«a (по имени автора, впервые его описавшего). В этих случаях обнаруживаются билатеральные, но несколько асимметричные очаги ушиба в конвекситальной коре.
Очаги ушиба различны по своей форме, величине, локализации, численности.
Л.И. Смирнов выделял следующие основные формы ушибов мозга:
1) крупные кортико-субкортикалъные очаги геморрагического размягчения с разрывами мягких мозговых оболочек;
2) пятна коркового геморрагического размягчения при целости мягких мозговых оболочек, захватывающие всю толщу коры;
3) геморрагическое размягчение толщи коры при сохранности молекулярного слоя;
4) внутрикорковые пластинчатые (слоистые) размягчения, локализующиеся в большинстве случаев в третьем-четвертом слоях коры;
5) очаги контузионного размягчения, осложненные надрывами твердой мозговой оболочки и внедрением костных осколков в мозговое вещество.
Для объективизации оценки степени повреждения мозга в 1985 году J. Adams с соавт. использовали так называемый контузионнътй индекс. Для этой цели измеряли глубину и ширину очага ушиба в различных участках мозга. При этом границы очага ушиба определялись микроскопически, т.к. неимбибированная кровью некротическая зона при макроскопическом изучении обычно бывает трудно различима. В результате проведенного исследования авторы показали, что:
а) ушибы мозга тяжелой степени чаще локализуются в лобной и височной долях, а также выше и ниже сильвиевой щели;
6) ушибы мозга тяжелой степени чаще являются результатом вдавленного перелома костей черепа;
в) независимо от того, приходился ли удар в лоб или затылок, ушиб мозга более тяжелой степени приходится на лобную долю;
г) при несоответствии клиники тяжелой ЧМТ макроскопически неизмененному мозгу (по данным КТ или аутопсии), проводили тщательное микроскопическое исследование, позволявшее выявить ДАП.
В 1994 году G. Ryan с соавторами, разработали метод количественной оценки степени ушиба мозга. Согласно предложенному протоколу, мозг после фиксации в формалине, разрезается на 116 секторов по предложенной схеме. Обнаруженные в каждом секторе макро- и микроскопические изменения фиксируются и наносятся на диаграммы, что позволяет детализировать информацию о распространенности повреждений в различных анатомических образованиях мозга и необходимо для изучения биомеханики ЧМТ.
Последовательные изменения очага ушиба подробно описаны в работах Л.И. Смирнова, R. Lindberg, Н.А. Сингур.
Очаг непосредственного разрушения ткани с кровоизлияниями окружен зоной необратимых и зоной обратимых изменений паренхимы мозга, являющейся источником тканевых реакций, обеспечивающих очищение очага и его организацию. В течение первых 3 сут зона ушиба представлена не-кротизированной тканью с кариорексисом, плазмолизом, очаговыми скоплениями лейкоцитов (рис. 9—4, 9—5). В это же время появляются первые зернистые шары-макрофаги. Активное врастание в зону некроза новообразованных сосудов (рис. 9—6) начинается через 6—7 сут. При этом важную роль в ангиогенезе и посттравматических процессах репарации играет повышенная экспрессия эндотелиального фактора роста сосудов.
Гистологическое исследование мозга умерших в течение 48 часов после ЧМТ, позволяет проследить динамику изменений в перифокальной зоне ушиба мозга на светооптическом уровне. Эозинофилия нейронов проявляется через I час после травмы, постепенно нарастая в интенсивности окраски и в количестве эозинофильных нейронов. Инкрустация нейронов выявляется в интервале между 3 и 48 часами. Не только ушиб мозга средней, но даже легкой степени приводит к отсроченным изменениям цитоскелета аксонов в различных областях мозга. Набухание аксонов постепенно нарастает в течение всего периода наблюдения (1 — 48 часов). Инфильтрация сегментоядерньши лейкоцитами, появляющимися уже через 10 минут после травмы мозга постепенно усиливается на протяжении 48 часов (в неосложненных случаях).
При ушибах мозга легкой степени организация некроза или кровоизлияния в коре начинается уже через 15 часов после травмы и может заканчиваться формированием очажка клеточного глиоза (рис. 9—7). Сращений твердой и мягкой мозговой оболочек над этими очагами обычно не бывает, но листки мягких мозговых оболочек срастаются.
При ограниченных субарахноидальных кровоизлияниях, не сопровождающихся нарушением целостности лептоменингса, в течение первых 5—7 сут происходит резорбция излившейся крови макрофагами. Кровоизлияние в поверхностные отделы коры приводит к очаговому разрушению концевых ветвей апикальных дендритов нейронов, расположенных в глубоких слоях коры; возможны некро-биотические изменения ассоциативных и вставочных нейронов П—IV слоев коры, наиболее ранимых при гипоксии, микроциркуляторных нарушениях.
| Рис. 9—8. Гомогенные массы в центре очага ушиба и отложения гемосидерина по его периферии. Окраска гемотоксилин-эозином, ув.х 100. | Рис. 9—9. Формирование пигментированного глиомезодермального рубца. Окраска гемотоксилин-эозином, ув.х 100. |
На месте ушиба мозга средней степени через 3—4 месяца обнаруживается рыхло петлистая сеть аргирофильных волокон и интенсивное развитие глиальных волокон, плотное срастание с мягкой мозговой оболочкой, нередко врастание соединительно-тканных волокон из мягкой мозговой оболочки в мозговую ткань. Интенсивное развитие глиальных волокон и гипертрофированные астроциты обнаруживаются по периферии глиомезодермального рубца.
При ушибах мозга тяжелой степени соотношение мозгового детрита и количества излившейся крови значительно варьируют. На протяжении 3—4 суток после травмы могут возникать эрозивные кровоизлияния, обусловленные фибриноидными некрозами стенок сосудов. Процессы организации значительно замедляются. Через 2 нед центральная часть очага занята гомогенной массой полужидкого распада ткани (рис. 9—8) с группами кристаллов гематоидина; зернистые шары располагаются лишь по периферии. Через 4—6 недель новообразованные сосуды врастают только в периферические отделы очага. В течение 3—5 месяцев и до 1,5 лет после травмы на месте очага ушиба тяжелой степени формируются пористые, компактные, кистозные, часто пигментированные глиомезодермальные рубцы (рис. 9—9) и посттравматические кисты, содержащие ксантохромную жидкость. Мягкие мозговые оболочки обычно сращены с твердой мозговой оболочкой.
Конечным исходом обширных очагов разрушения мозговой ткани являются кисты, окруженные зоной аргирофильных и коллагеновых волокон, в свою очередь, окаймленную поясом волокнистого глиоза. В прилежащих участках коры через многие годы можно найти инкрустированные кальцием нейроны, а в белом веществе дистрофические изменения в виде спонгиозного его состояния и образования миелиновых шаров, что макроскопически выражается в атрофии ипсилатерального полушария, преимущественно белого вещества, и вент-рикуломегалии бокового желудочка. Нередко обнаруживаются так называемые старческие бляшки, содержащие бета-амилоид, аналогичные бляшкам в мозге пациентов с болезнью Алъцгсймера.
ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ
Механическое разрушение клеток мозга оказывается первой ступенью, ведущей к истечению внутриклеточных ионов и последующей активации генов, появлению свободных радикалов и перекисному окислению липидных клеточных мембран. Повышение уровня внутриклеточного кальция, активация фосфолипаз и кальлейна способствуют вторичному повреждению клеточных мембран и цитоскелета, затруднению транспорта аксоплазмы и как следствие этого — отсроченной гибели клетки.
При экспериментальной травме локальным воздействием на кору мозга крысы в течение 25 миллисекунд первичное геморрагическое повреждение наблюдается на месте приложения силы. Через 3 дня после травмы патология аксонов выявляется в субкортикальном белом веществе и во внутренней капсуле поврежденного полушария.
На формирование очага ушиба мозга, на ранних стадиях ЧМТ, существенное влияние оказывают развивающаяся при этом распространенная цереброваскулярная патология, включая субарахноидальное кровоизлияние, очаговые стазы (аккумуляция тромбоцитов) и тяжелая ишемия. Через 30 минут после экспериментального очагового повреждения мозга (током жидкости в 1,7—2,2 атмосфер) обнаруживается стаз крови в пиальных сосудах над очагом повреждения и снижение кровотока в этой зоне. Умеренное снижение кровотока наблюдается и в других участках поврежденного полушария, включая лобную и височную доли, гиппокамп, таламус и чечевичное ядро; легкое снижение кровотока происходит и в коре противоположного полушария.
Повреждение мозга запускает каскад воспалительных клеточных реакций и сама травма мозга является ключевым фактором в развитии острой посттравматической воспалительной реакции. Повышенная экспрессия таких цитокинов, как туморонекротический фактор — альфа (TNF-alpha) и интерлейкин, появляется только при тяжелой травме мозга и в первые 4 часа в поврежденной коре.
Развитию вторичных посттравматических повреждений и дисфункций мозга способствует также и апоптоз клеток. Значительно меньше, по сравнению с нейронами, обнаруживается фрагментация ДНК в астроцитах. Уже через 2 часа после ушиба выявляется фрагментация ДНК во всех нейронах в коре — зоне ушиба и сохраняется, по меньшей мере, 2—4 недели. Апоптоз обнаруживается также в нейронах ипсилатерального гиппокампа и зернистом слое зубчатого ядра мозжечка, т.е. на существенном расстоянии от очага ушиба.
Через 3 дня после локального экспериментального ушиба коры больших полушарий мышей, выявляется экспрессия c-jun РНК (постоянного маркера нейронов, реагирующих на стресс или повреждение) в клетках Пуркинье обеих полушарий мозжечка, а через 1 неделю и в черве мозжечка. Механизм воздействия очага ушиба коры больших полушарий мозга на мозжечок остается пока неясным. Высказывается предположение о транснейрональной активации генов.
Повреждение клеток при травме мозга не только запускает воспалительные клеточные реакции, но и вызывает экспрессию различных тРНК, способствующих усилению адаптивных свойств ткани мозга. Через 30 минут после экспериментального ушиба мозга повышается экспрессия тРНК глиофибриллярного кислого белка (ГФКБ), что свидетельствует об активации астроцитов. Первые 2 часа после травмы мозга активация тРНК астроцитов выявляется в перифокальной зоне, тогда как через 24 часа этот процесс распространяется на не только на все поврежденное полушарие, но обнаруживается и в гиппокампе и коре противоположного полушария. Иммуногистохимический метод выявляет реактивные астроциты через 1—3 сут и периконтузионно в зоне ушиба, в белом веществе и гиппокампе поврежденного полушария. Наряду с этим, в перифокальной зоне очага ушиба через 3 часа после травмы мозга отмечается повышенная экспрессия АРР-белка предшественника амилоида, необходимого для восстановления структуры миелина. Повышенная экспрессия АРР сохраняется в течение последующих 3 сут, возможно и более длительный период.
Одним из постоянных компонентов ушиба мозга является вазогенный и/или цитотоксический отек. Существует прямая связь между нарушением микроциркуляции, с последующим увеличением уровня внеклеточного лактата, истечением внутриклеточного калия и развитием цитотоксического отека. Нарушение регуляции межклеточной адгезивной молекулы-1 в стенках сосудах обнаруживается после ушиба мозга не только вокруг очага повреждения, но и на значительном от него расстоянии, в неповрежденных сосудах, что способствует посттравматической адгезии лейкоцитов, нарушениям микроциркуляции и отеку мозга. Через 5 минут после экспериментального вакуумного ушиба мозга, при электронно-микроскопическом исследовании виден отек эндотелиальных клеток; нарушений межклеточных контактов в это время нет.
Используя иммуногистохимические маркеры острого воспалительного процесса, такие как идентификация нейтрофилов (моноклональные антитела RP-3) и молекулы адгезии эндотелия (Е-selectin), еще раз экспериментальным путем было доказано, что в случаях ушиба мозга (в отличие от ДАП) раннее нарушение гематоэнцефалического барьера, наблюдаемое через 1 час после траимы мозга, связано с воспалительной реакцией. Независимо от особенностей экспериментальных методик нанесения травмы мозга, выраженный отек мозга развивается через 2 часа и первичной движущей силой скопления жидкости в очаге ушиба мозга, является повышенный коллоидно-осмотический потенциал некротизированной ткани.
Воспалительные и регенераторные процессы после травмы мозга длятся в течение длительного времени, вплоть до 1 года после экспериментальной травмы мозга крыс. В неосложненных случаях нейтрофильная инфильтрация поврежденной ткани продолжается не более одной недели, тогда как макрофаги, обнаруживаемые в очаге повреждения через 48 часов после травмы, сохраняются, по крайней мере, в течение 1 года. Механическое повреждение мозга индуцирует комплекс клеточных и молекулярных реакций, выражающийся, в том числе, и реактивным глиозом. В интервале от 3 до 14 сут после экспериментального ушиба мозга определяется повышенная экспрессия рецептора бензодиазина, локализованного на наружной мембране митохондрий астроцитов и микроглии и транспортирующего холестерол к месту биосинтеза нейростероида, что сопровождается компенсаторным увеличением количества (гиперплазией) этих клеток.
Значительное увеличение числа астроцитов (иммуноположительных при окрашивании ГФКБ) обнаруживается вплоть до 4 недель. Через 30 сут после ушиба мозга экспрессия тРНК ГФКБ наблюдается во всех отделах белого вещества поврежденного полушария, однако и в течение последующих недель, вплоть до 1 года может увеличиваться количество астроцитов. Регенерация дендритов, выявляемая специальными иммуногистохимическими маркерами повреждения дендритов в перифокальной зоне, проявляется только через 2 месяца после травмы, но сохраняется в течение исследованного года, что свидетельствует о параллельно протекающих компенсаторных процессах.
Экспериментальные исследования показывают возможности патогенетического лечебного воздействия на поврежденный мозга. От 3 часов до 3 сут после травмы мозга при нормальной температуре тела большое число сегментоядерных лейкоцитов выявляется периваскулярно в поврежденной ткани и субарахноидальном пространстве. Гипотермия (30,0°С) и гипертермия (39,0°С) значительно влияют на активность лейкоцитов. Посттравматическая гипотермия снижает активность лейкоцитов не только в поврежденной, но и неповрежденной (контрольной) коре, тогда как гипертермия повышает активность лейкоцитов только в поврежденной коре. Таким образом, посттравматическая гипотермия уменьшает активность лейкоцитов не только в ранние часы после травмы (3 часа), но и в течение последующих нескольких сут.
Известно, что кортикотропин — рилизинг фактор, гипоталамический нейропептид, ингибирует трансэндотелиальное истечение плазмы. Введение животным, с экспериментально полученным ушибом мозга, 50 и 100 микрограмм/кг кортикотропинрилизинг фактора уменьшает травматический отек мозга, снижая проницаемость гематоэнцефа-лического барьера.
Введение антагонистов туморонскротического фактора (TNF alpha) в желудочки мозга за 15 минут до нанесения травмы и через 1 час после экспериментальной травмы мозга, улучшает посттравматическую двигательную активность, тогда как внутривенное введение этого же вещества не оказывает аналогичного воздействия .
В качестве контроля за процессами организации очага ушиба мозга могут служить данные об уровне концентрации в сыворотке крови маркеров повреждения глии (S-100) и нейронов (NSE). Так, уровень концентрации маркеров коррелирует с объемом очага ушиба, определяемым по данным КТГ.
Таким образом, многочисленные экспериментальные исследования ушиба мозга показали, что характер распространения вторичных изменений зависит не только от наличия самого очага повреждения, но и механизма получения травмы мозга. Именно комбинированное воздействие на мозг механического разрушения в сочетании с нейроток-‘ сическим воздействием некротизированной ткани обусловливает патологию, наблюдаемую в посттравматическом периоде. Кроме того, что не менее важно, показана возможность патогенетического лечебного воздействия с целью предупреждения или ослабления вторичных повреждений ткани мозга.
КЛИНИКА
Топические варианты расположения ушибов и раз-мозжений мозга исключительно разнообразны и, соответственно, вариабельна клиника. Все же представляется оправданным изложение их семиотики с учетом главных мест локализации.
Повреждения лобной доли
До 40—50% очаговых повреждений вещества головного мозга локализуется в лобных долях (рис. 9— 10, 9-11, 9-12, 9-33, 9-14, см. рис. 9-25) . Это обусловлено: во-первых, значительностью их массы — лобные доли по своему объему превосходят все иные отделы мозга, во-вторых, особой подверженностью лобных долей как ударной (при приложении травмирующего агента к лобной области), так и, особенно, противоударной ударной (при приложении травмирующего агента к затылочной области) травме.
Рис. 9—10. Множестьенные очаги ушиба средней степени в базальных отделах левой лобной доли и кортикально-субкортикальные в левой височной доле. МРТ. Аксиальные томограммы: А — по Т1, Б — по Т2.
Рис. 9—11. КТ динамика ударно-противоударных очагов ушиба в левой теменной и правой лобной долях. КТ динамика. А, Б — при поступлении. В, Г — через 37 суток. На месте ударного очага сформировался участок локальной атрофии вещества головного мозга, на месте противоударного — гетероденсивная зона, отражающая формирование рубцово-атрофического процесса.
Благодаря своей массе и сравнительной удаленности, особенно передних отделов (в сопоставлении с височными долями), от ствола мозга, лобным долям часто присуща возможность длительно «амортизировать» масс-эффектдаже при их крупноочаговых повреждениях. Этому способствует также саногенный сброс избыточной жидкости вместе с продуктами распада через формирующиеся «дорожки» из очагов размозжений в передние рога боковых желудочков.
При повреждениях лобных долей общемозговая симптоматика представлена угнетением сознания в пределах оглушения, сопора или комы (в зависимости от тяжести ушиба). Нередко характерно развитие внутричерепной гипертензии с интенсивной головной болью, многократной рвотой, психомоторным возбуждением, брадикардией, появлением застоя на глазном дне (особенно при базалъных повреждениях). При массивных очагах размозжения с выраженным перифокальным отеком может развиваться аксиальное смещение с возникновением вторичных среднемозговых симптомов (парез взора вверх, спонтанный нистагм, двусторонние патологические знаки и др). При повреждениях лобных долей особенно часты нарушения сна и бодрствования с их инверсией: возбуждение ночью и сонливость днем.
Рис. 9—12. Множественные ушибы лобных долей у пострадавшего 31 года. КГ динамика. А, Б — при поступлении. Множественные гиперденсивные участки, чередующиеся с гиподенсивными в лобных долях. В, Г — через 9 суток. Гомогснногиподенсивныс зоны в обеих лобных долях. Д, Е — 31-е сутки. Четко выявляются зоны формирования атрофического процесса в местах разрешения контузионпых очагов при нормализации размеров боковых желудочков. МРТ через 10 суток после травмы в режимах Т1 (Ж, 3) и Т2 (И, К). Участки повышения сигнала в лобных долях имеют высокую контрастность изображения и четкие контуры, что отражает наличие дериватов окисления гемоглобина в контузионных очагах (по данным КТ на 9-е сутки превратившихся из гиперденсивных в гиподенсивные).
Рис. 9—13. Очаг размозжения в левой лобной доле при вдавленном переломе у 30-летнего пострадавшего. КТ. А, Б, В, Г аксиальные срезы.
Для ушибов лобных долей тяжелой степени характерна выраженность менингеальных симптомов с частым преобладанием, по мере санации ликвора, симптома Кернига над ригидностью мышц затылка.
Среди очаговых признаков доминируют нарушения психики, которые проявляются тем ярче, чем меньше угнетено сознание. Часто встречаются нарушения сознания по типу его дезинтеграции. При поражении левой лобной доли возможны сумеречные состояния сознания, психомоторные припадки, абсансы с амнезией на них. При поражении правой лобной доли основное место занимают конфабуляции или конфабуляторная спутанность. Часты изменения в эмоционально-личностной сфере. В рамках дезинтеграции сознания могут проявляться дезориентировка в собственной личности, месте и времени, негативизм, сопротивление осмотру, отсутствие критики к своему состоянию, стереотипии в речи, поведении, эхолалия, персеверация, булемия, жажда, неопрятность, нарушение контроля над функциями тазовых органов и т.п. Следует учитывать, что в первых 7—14 сут после ЧМТ нередко наблюдается волнообразность угнетения сознания в пределах оглушения-сопора с эпизодами спутанности и психомоторного возбуждения.
Рис. 9—14. Пострадавшая 30-лет с тяжелой ЧМТ. Вдавленный перелом костей свода черепа справа с подлежащим контузионньш очагом 1? лобной доле. А — трехмерная КТ реконструкция демонстрирует топографическое соотношение мягких тканей, костей черепа и мозговых структур. Б — трехмерное КТ изображение полушарий дает представление о распространенности повреждения коры мозга.
У пострадавших с алкогольным анамнезом на 2—5-е сут после ЧМТ может развиваться делириозное состояние со зрительными и тактильными галлюцинациями. ‘
По мере отдаления от момента травмы и условного прояснения сознания (выход из оглушения) четче проявляются межполушарные и локальные особенности нарушений психики при повреждениях лобных долей.
У пострадавших с преимущественным поражением правой лобной доли чаще отмечаются признаки снижения личности (страдает критика к своему состоянию, апатия, склонность к благодушию и другие проявления упрощения эмоциональных реакций), снижение инициативы, памяти на текущие события. Часто проявляются эмоциональные расстройства различной степени выраженности. Возможны эйфория с расторможенностью, крайняя раздражительность, немотивированные или неадекватные вспышки гнева, злобы (синдром гневливой мании).
У пострадавших с поражением доминантной (левой) лобной доли могут выявляться речевые нарушения по типу моторной афазии (эфферентной — при поражении нижних отделов премоторной области), диемнестические явления при отсутствии выраженных расстройств восприятия пространства и
времени (что более характерно для поражений правой лобной доли).
При двухстороннем повреждении лобных долей к упомянутым нарушениям психики добавляются (или усугубляются) отсутствие инициативы, побуждений к деятельности, грубая инертность психических процессов, утрата социальных навыков часто на фоне абулической эйфоризации. В ряде случаев развивается псевдобульбарный синдром.
Для лобно-базальных повреждений типична одно или двухсторонняя аносмия в сочетании с эйфорией или эйфорической расторможенностью, особенно при поражении правой лобной доли.
При конвекситальной локализации повреждений лобных долей характерны центральные парезы лицевого и подъязычного нервов, контрлатеральные моно- или гемипарезы конечностей, особенно лингвофациобрахиальные парезы в сочетании со снижением инициативы вплоть до аспонтанности (что при поражении левой лобной доли ярко выступает в сфере психомоторики и речи).
Для поражения передних отделов лобной доли типична диссоциация между отсутствием пареза лицевой мускулатуры при выполнении инструкций («оскальте зубы» и т.п) и четким парезом тех же мышц в мимике (мимический парез лицевого нерва).
При повреждениях, захватывающих экстрапирамидные отделы лобных долей, часто встречается симптом противодержания. При проверке врачом пассивных движений в конечностях, либо в шее, возникает непроизвольное напряжение мышц-антагонистов, создающее впечатление сознательного сопротивления больного.
За счет нарушения лобно-мосто-мозжечковых путей при очаговых повреждениях лобной доли характерна туловищная атаксия с невозможностью сидеть, стоять и ходить (астазия-абазия), при этом тело отклоняется в сторону, противоположную поражению.
При фронтальных ушибах нередко возникают эпилептические припадки — общие (полюс лобной доли), адверзивные (прсмоторная зона), фокальные судорожные приступы с дальнейшей генерализацией (передняя центральная извилина).
При очаговых повреждениях лобных долей почти всегда выявляются хватательные рефлексы, хоботковый рефлекс, а также другие симптомы орального автоматизма.
В зависимости от степени повреждения дорзо-латеральной, префронтальной, орбитофронтальной или медиофронтальной коры и их связей со зрительным бугром, хвостатым ядром, бледным шаром, черной субстанцией и другими подкорковыми и стволовыми образованиями меняется структура симптоматики ушибов лобной доли.
Повреждения височной доли
Височная доля — весьма уязвимое при ЧМТ образование мозга. На височные доли приходится до 35%—45% всех случаев очаговых повреждений мозга (рис. 9-15, 9-16, 9-17, см. рис. 9—24). Это объясняется особенно частым приложением травмирующего агента к височной области, страданием височных долей по механизму противоудара при почти любой локализации первичного воздействия механической энергии на голову, анатомическими условиями (тонкая чешуя височной кости, расположение основной массы доли в средней черепной яме, ограниченной костно-дуралъными выступами, непосредственное прилегание к стволу мозга). В результате височные доли, вслед за лобными, также относятся к «излюбленным» местам расположения очагов ушиба и размозжения мозга.
Общемозговыс симптомы при повреждениях височных долей схожи с таковыми при повреждениях других долей мозга: изменения сознания от умеренного оглушения до глубокой комы; головная боль с тошнотой, головокружением, рвотой; застойные явления на глазном дне; психомоторные вспышки и т.п.
Рис. 9—15. Множественные кортикально-субкортикальные очаги ушиба средней степени в левой височной доли. МР- томограммы, аксиальные А — Т1, Б — Т2, В — фронтальная по Т1.
Рис. 9—16. Множественные очаговые повреждения головного мозга у пострадавшего 45 лет. МРТ в режиме Т1. А, Б — ударные парасагиттальные ушибы. В — противоударный очаг ушиба в базальных отделах височной доли слева. Г — на фронтальной томограмме дополнительно выявляется небольшая субдуральная гематома слева.
Однако в силу анатомической близости височных долей к оральным отделам ствола и гипоталамуса повышение внутричерепного давления при их очаговых повреждениях может быстрее и резче обусловливать жизненно опасные дислокации мозга. «Амортизирующая» роль значительного слоя вещества мозга, смягчающего воздействие на ствол очаговых повреждений лобных, теменных или затылочных долей, здесь много меньше. Поэтому в клиническую картину повреждений височных долей больше, чем при иной локализации ушибов мозга, вплетаются вторичные стволовые симптомы. В основном, речь идет о смещениях орального отдела ствола в случаях увеличения объема пораженной височной доли и проникновения крючка гиппокампа в тенториальное отверстие. Промежуточный и средний мозг смещается контрлатерально от патологического очага, травмируется о противоположный край мозжечкового намета, при этом нередко развиваются вторичные дисгемии в стволе и аксональное повреждение проводниковых систем.
Дислокационный среднемозговой синдром при повреждении височной доли проявляет себя анизокорией, вертикальным нистагмом, парезом взора вверх, двусторонними патологическими стопными знаками, гомолатеральными парезами конечностей, за которыми следуют грубые диффузные нарушения мышечного тонуса и угрожающие расстройства жизненно важных функций. Острые дислокации и деформации ствола чрезвычайно опасны для жизни пострадавшего. При подострых или медленно нарастающих дислокациях имеется больше возможностей для их купирования.
Рис. 9—17. Очаг размозжения в височной доле справа. Консервативное лечение. КТ-динамика. Верхний ряд — при поступлении на первые сутки после ЧМТ. Очаг размозжения сопровождают множественные мелкие геморрагии в глубинных структурах. Диффузный отек обоих полушарий. Средний ряд — пятые сутки после ЧМТ. Нарастание отека мозга. Появление дополнительных геморрагии. Нижний ряд — через 2 мес после ЧМТ. Разрешение очага размозжения и мелких геморрагии с исходом в грубую локальную и умеренную диффузную атрофию. Хорошее клиническое восстановление.
Ряд вегетативных и висцеральных расстройств, однотипных с медиально-височными, встречается и при смещении диэнцефальньгх структур, при этом также наблюдаются нарушения ритма сна, терморегуляции, сосудистой микроциркуляции; могут развиваться горметонические судороги.
Из вторичных симптомов при повреждениях височной доли реже и слабее выражены синдромы моста и продолговатого мозга.
Среди локальных признаков повреждений височных долей доминантного (обычно левого) полушария обращают внимание явления сенсорной афазии — от затруднения понимания сложных оборотов обращенной речи до полной утраты анализа как слышимой, так и собственной речи, что образно обозначается как «словесная окрошка». В промежуточных степенях сенсорной афазии наблюдаются литеральные и вербальные парафазии; дефекты слухо-речевой памяти, опознавания и воспроизведения: сходных по звучанию фонем в слогах и словах, отчуждение смысла слов. При поражении угловой извилины, находящейся на стыке с теменной и затылочной долями, т.е. зоны, интегрирующей слуховую, зрительную и сенсорную афферентацию, развиваются алексия, аграфия, акалькулия. Повреждение аналогичных зон субдоминантного (обычно правого) полушария обусловливает нарушение узнавания и Боспроизведения «первосигнальных» звуков — бытовых, уличных, природных шумов, а также знакомых мелодий, интонационного и эмоционального строя речи, что можно проверить, если позволяет общее состояние пострадавшего.
Повреждение задней трети нижней височной извилины служит причиной развития амнестической афазии, хотя этот симптом после ЧМТ может выступать и как общемозговой, особенно у лиц пожилого возраста.
Глубинные контузионные очаги вызывают контрлатеральную гомонимную гемианопсию: нижнеквадрантную — при избирательном поражении зрительного пути, идущего над нижним рогом бокового желудочка, и верхнеквадрантную — при поражении этого пути под нижним рогом.
Выраженность контрлатеральных парезов конечностей при повреждениях височной доли зависит от того, насколько они близки к внутренней капсуле.
Часто наблюдаются мелкий спонтанный горизонтальный нистагм, бьющий в сторону поражения, а также явления височной атаксии.
Целая гамма вегетативно-висцеральных симптомов может возникнуть при поражении медиального отдела височной доли, причем не только при первичном ее повреждении, но и вследствие вклинения в тенториальное отверстие гиппокампа с его крючком в случае объемного увеличения височной доли. Ирритация древней коры обусловливает сбои в регуляции висцеральных и вегетативных функций, что реализуется как субъективными (ощущение тяжести, дискомфорта, слабости, замирания сердца, жара и т.п.), так и объективными симптомами (нарушение сердечного ритма, ангиозные приступы, метеоризм, гиперемия или бледность покровов и т.п.). Меняется фон психического состояния пострадавшего с преобладанием отрицательных эмоций, чаще по типу скованной депрессии. Наряду с этим могут отмечаться пароксизмы страха, тревоги, тоски, дурных предчувствий. Наиболее заметны для больного нарушения вкуса и обоняния в виде извращенного восприятия и обманов. Медиально-височные ушибы, особенно в отдаленном периоде, нередко проявляются исключительно эпилептическими припадками или их эквивалентами. В качестве последних могут выступать обонятельные и вкусовые галлюцинации, сенсорно-висцеральные пароксизмы, вестибулярные атаки, состояния «ранее виденного»; относительно редки классические «потоки воспоминаний» при височной эпилепсии. Эпилептические приступы возможны и при повреждении конвекситальных отделов височной доли; в качестве эквивалентов или ауры тогда выступают простые либо сложные (с развернутой речью) слуховые галлюцинации.
Повреждения теменной доли
Несмотря на значительный объем теменной доли, ее повреждения встречаются гораздо реже (рис. 9— 18, см. рис. 9—11), чем вещества лобной или височной долей. Это обусловлено топографией, благодаря которой теменные доли обычно испытывают лишь ударную травму, а противоударный механизм их повреждений почти полностью выпадает. Однако по этой же причине здесь часты ушибы мозга, обусловливаемые вдавленными переломами.
Теменная доля — единственная из всех долей мозга, не имеющая базальной поверхности. Сравнительная ее удаленность от стволовых образований — причина более медленного темпа и более мягкого развертывания среднемозгового дислокационного синдрома даже при обширных очагах размозжения. Краниобазальная симптоматика при ушибах теменных долей всегда вторична.
Рис. 9—18. Ушиб головного мозга средней степени (геморрагический ушиб). КТ динамика: верхний ряд — при поступлении. В теменной и отчасти височной долях слева кортикально-субкортикально, некомпактно расположены участки геморрагического пропитывания, окруженные перифокальпым отеком с умеренным объемным эффектом. Средний ряд: 9-е сутки после ЧМТ. Снижение плотности очагов геморрагии, больше в глубинных отделах. Сохраняется перифокальный отек. Нижний ряд: спустя 1 месяц после ЧМТ. В зоне геморрагического ушиба определяются умеренные очаговые изменения (гипо-денсивный участок). Признаки легкой диффузной атрофии. Хорошее восстановление.
К первичногнездным признакам повреждения теменной доли относятся: контрлатеральные нарушения болевой, а также глубокой чувствительности, парестезии, нижнеквадрантная гомонимная гемианопсия, одностороннее снижение или выпадение роговичного рефлекса, парезы конечностей с афферентным слагаемым, а также нарушение бинаурального слуха. При повреждениях теменной доли могут развиваться фокальные сенситивные эпилептические пароксизмы.
Наряду с перечисленными локальными признаками, свойственными и левой, и правой теменным долям, имеются и различия в семиотике повреждений каждой из них у праворуких. При левосторонних повреждениях могут обнаруживаться амнести-ческая афазия, астереогноз, пальцевая агнозия,
апраксия, нарушения счета, вербального мышления, иногда и неточности ориентировки в пространстве и времени. При правосторонних повреждениях — проявляются расстройства эмоциональной сферы с тенденцией к преобладанию благодушного фона, неосознавание своего болезненного состояния, двигательных, зрительных и иных дефектов; возможно развитие левосторонней пространственной агнозии, когда больные игнорируют или слабо воспринимают происходящее слева от них; этому может сопутствовать гемисоматоагнозия, псевдопо-лимелия (вместо одной левой руки воспринимают несколько, нередко различая среди них собственную).
Повреждения затылочной доли
В силу небольшого объема затылочных долей, а также амортизирующей роли намета мозжечка очаговые повреждения встречаются здесь намного реже, чем в других долях мозга. Очаги ушиба и раз-мозжения обычно возникают при импрессионной травме затылочной области.
В клинике повреждений затылочной доли преобладает общемозговая симптоматика. При одностороннем повреждении медиальной поверхности затылочной доли среди очаговых признаков характерна контрлатеральная гомонимная гемианапсия, а при билатеральном поражении — снижение зрения на оба глаза с концентрическим сужением полей зрения вплоть до корковой слепоты. При повреждении конвекситальных отделов затылочных долей наблюдается зрительная агнозия — неузнавание предметов по их зрительным образам. Иногда возникают метаморфопеии — искаженное восприятие формы наблюдаемых предметов, которые, кроме того, могут казаться или слишком маленькими (микропсия) или слишком большими (макропсия). При раздражении коры затылочной доли пострадавший может ощущать вспышки света, цветные искры или более сложные зрительные образы.
Пирамидные симптомы нехарактерны для повреждений затылочной доли, вместе с тем — за счет нарушения функций затылочно-мосто-мозжечкового пути — может проявляться атаксия в контрлатеральных конечностях. При страдании затылочного коркового центра взора развиваются горизонтальные парезы взора в противоположную сторону, которые выражены обычно в меньшей степени, чем при поражении лобного коркового центра взора.
Повреждения подкорковых узлов
Современные возможности прижизненной диагностики травматического поражения мозга с помощью КТ и МРТ, опыт клинической неврологии и нейро-морфологии расширили представления о повреждениях подкорковых узлов. Наиболее типичными причинами их дисфункции при ЧМТ являются следущие: 1) непосредственное повреждение подкорковых узлов в результате ушиба и размозжения мозга, внутри мозговых и внутрижелу-дочковых гематом, а также отека и дислокации, вторичной ишемии; 2) нарушение функций подкорковых узлов при диффузной аксоналъной дегенерации; 3) изменение функционального состояния подкорковых узлов без деструкции в связи с нарушением рецепторных аппаратов и систем, обеспечивающих нейромедиаторную регуляцию двигательных функций; 4) формирование в подкорковых узлах генераторов возбуждения и детерминантных очагов.
Функциональная гетерогенность подкорковых узлов обусловливает необычайное многообразие их клинических синдромов. Они присутствуют в остром периоде тяжелой ЧМТ, сохраняются в течение длительного времени после комы; всегда определяются в вегетативном состоянии. Наиболее типичны: 1) различные варианты стойких позно-тонических реакций (декортикация, децеребрация, эмбриональная поза и др); 2) преходящие тонические судороги, 3) гиперкинезы с тенденцией к стереотипным ритмическим двигательным актам (бросковыс движения рук, повороты туловища, автоматическая ходьба, паракинезы); 4) диффузное, хаотическое двигательное возбуждение.
Характерны сочетанные проявления подкорковых феноменов (позно-тонические реакции с хореоатетозом, тремором, штопорообразными движениями туловища, типичные изменения мышечного тонуса), нередко с висцеральновегетативными и аффективными реакциями.
В посткоматозном периоде чаще отмечается ограниченность движений, амимия, диффузное повышение мышечного тонуса, тремор в покое и при статическом напряжении (паркинсоноподобные синдромы). О поражении подкорковых узлов могут также свидетельствовать яркие симптомы орального автоматизма.
Повреждения мозжечка
Ушибы мозжечка доминируют среди повреждений образований задней черепной ямки (рис. 9— 19). Очаговые повреждения мозжечка обычно обусловлены ударным механизмом травмы (приложение механической энергии к затылочно-шейной области при падении на затылок либо ударе твердым предметом), что подтверждается частыми переломами затылочной кости ниже поперечного синуса.
Рис. 9—19. Очаговый ушиб левого полушария мозжечка. МРТ. Аксиальные томограммы: А — по Т1, Б — по Т2, В — фронтальная томограмма.
Общемозговая симптоматика (нарушения сознания, головная боль, брадикардия и др) при повреждениях мозжечка часто имеет окклюзионную окраску (вынужденное положение головы, рвота при перемене положения тела в пространстве, раннее развитие застойных сосков зрительных нервов и др.) в связи с близостью к путям оттока ЦСЖ из головного мозга.
Среди очаговых симптомов при ушибах мозжечка доминируют односторонняя либо двусторонняя мышечная гипотония, нарушения координации, крупный тонический спонтанный нистагм. Характерна локализация болей в затылочной области с иррадиацией в другие области головы. Часто одновременно проявляется та или иная симптоматика со стороны ствола мозга и черепных нервов. При тяжелых повреждениях мозжечка возникают нарушения дыхания, горметония и другие жизненно опасные состояния.
Вследствие ограниченности субтенториального пространства даже при сравнительно небольшом объеме повреждений мозжечка нередко развертываются дислокационные синдромы с ущемлением продолговатого мозга миндалинами мозжечка на уровне затылочношейной дуральной воронки либо ущемлением среднего мозга на уровне отверстия мозжечкового намета за счет смещаемых снизу вверх верхних отделов мозжечка.
Повреждения ствола мозга
Первичные повреждения ствола мозга редки (рис. 9—20, 9—21). При разрывах ствола пострадавшие обычно погибают на месте ЧМТ. Ограниченные ушибы ствола встречаются при переломах основания черепа (ударная травма) и при падении на спину (механизм противоударной травмы). При угловом ускорении мозга в момент травмы может повреждаться мезэнцсфальный отдел ствола.
При ушибах среднего мозга у пострадавших появляются избирательно или в сложном сочетании синдромы: четверохолмный, тегментарный («покрышечный»), педункулярный («ножковый»), а также ряд альтернирующих синдромов поражения образований одной половины среднего мозга.
Четвсрохолмные симптомы включают нарушения взора вверх и вниз, разностояние глаз по вертикальной оси, расстройства конвергенции, двусторонние нарушения фотореакций, вертикальный, диагональный или конвергирующий нистагм.
Тегментарные симптомы включают в себя нарушения функций III и IV черепных нервов, причем возможно поражение лишь части глазодвигательных ядер, что выражается парезами отдельных глазодвигательных мышц.
Рис. 9—20. Очаг ушиба в стволе головного мозга на уровне покрышки среднего мозга и верхнего отдела моста слева. МР-томограммы. А — сагиттальная по Т1, Б — аксиальная по Т2. Артефакт от инородного тела в задних отделах правой височно-затылочной области.
Рис. 9—21. Ушиб ствола мозга. МРТ. Аксиальные томограммы. А — по TI, Б — по Т2. На фоне небольшого увеличения объема среднего мозга в покрышке среднего мозга и левой ножке мозга выявлена зона изменения сигналов, отражающих деструкцию вещества с элементами геморрагического пропитывания.
Возможны проводниковые нарушения всех видов чувствительности. Разнообразно изменяется мышечный тонус — за счет поражения связей красного ядра и черной субстанции. Одновременно расстраивается и координация движений, причем координаторные нарушения в конечностях контрлатсральны стороне патологии покрышки. Распространенное повреждение образований покрышки среднего мозга обусловливает развитие децерсбращюнной ригидности с параллельным нарушением сознания, возникновением гипертермии и патологических ритмов дыхания.
Педункулярный синдром представлен контрлатеральными нарушениями движений, при этом возможны и монопарезы, т.к. в ножках мозга сохраняется соматотопическое представительство пирамидного пути.
При ушибах мозга моста в клинике проявляются различные варианты гомолатеральных поражений отводящего, лицевого и двигательной порции тройничного нервов в сочетании с контрлатеральными парезами конечностей и нарушениями чувствительности. Характерен спонтанный нистагм, а также горизонтальные парезы взора. Встречаются и псевдобульбарные явления.
Непосредственное повреждение продолговатого мозга обусловливает клиническое проявление первичного бульбарного синдрома: нарушения функций тройничного (по сегментарному типу), языкоглоточного, блуждающего, добавочного и подъязычного нервов (дисфагия, дисфония, дизартрия, выпадение глоточного рефлекса), пирамидные симптомы вплоть до тетрапареза, координаторные и чувствительные расстройства. Характерен ротаторный нистагм.
ДИАГНОСТИКА
Распознавание повреждений вещества лобных долей строится на учете биомеханики травмы, выявлении на фоне внутричерепной гипертензии характерных нарушений психики, аносмии, симптомов орального автоматизма, мимического пареза лицевого нерва и др. признаков поражения передних отделов мозга. Краниография объективизирует вдавленные переломы и повреждения костных структур передних отделов основания черепа. КТ и МРТ дают исчерпывающую информацию о характере травматического субстрата, его внутридолевой локализации, выраженности перифокального отека, признаках аксиальной дислокации ствола и т.д.
Диагностика повреждений вещества височных долей базируется на анализе механизма ЧМТ, сочетания первичных очаговых и вторичных дислокационных симптомов. Однако в условиях экстренной диагностики зачастую не удается распознать повреждение правой (субдоминантной) височной доли, а наличие общемозговых и стволовых симптомов вообще может направить топический диагноз по ложному пути. Неоценимую помощь оказывают КГ и МРТ; при их отсутствии травматический процесс помогает латерализовать эхоэнцефалография. Определенную ценность сохраняет рентгенография черепа.
Распознавание повреждений вещества теменной доли у пострадавших, доступных контакту, базируется на выявлении нарушений чувствительности, афферентных парезов и других характерных симптомов с учетом места приложения травмирующего агента к голове. При глубоком оглушении, не говоря уже о сопоре и тем более коме, признаки поражения теменной доли по существу невозможно выявить. В этой ситуации решающая роль в топической диагностике принадлежит КТ и МРТ, а в случаях вдавленных переломов — краниографии.
Диагностика очаговых повреждений вещества затылочной доли строится на учете биомеханики травмы (особенно при ударе по затылочной области) и выявлении в качестве ведущего симптома контралатеральной гомонимной гемианопсии. КТ и МРТ хорошо визуализируют ушибы и размозжения затылочной локализации.
При распознавании очаговых повреждений подкорковых образований, особенно у пострадавших с нарушенным сознанием, необходимо ориентироваться на сопоставление неврологических и КТ-М РТ данных. В промежуточном и отдаленном периодах на основании тщательного клинического анализа обычно удается не только констатировать поражение подкорковых узлов, но и часто уточнять, какого именно. Гемигипестезия всех видов чувствительности (не только болевой, но и глубокой, тактильной, температурной) в сочетании с гиперпатией и тем более в сопровождении гемианопсии и гемиатаксии указывает на патологию зрительного бугра. Акинетическиригидный синдром свидетельствует о преимущественном поражении бледного шара и черной субстанции. Гипотонически-гиперкинетический синдром более характерен для поражения полосатого тела; гемибализм развивается при заинтересованности в процессе субталамического ядра.
При распознавании ушибов образований задней черепной ямки выявление односторонних нарушений координации в конечностях, гипотония в них, крупного спонтанного нистагма, указывают на поражение гомолатерального полушария мозжечка. Асинергия, туловищная атаксия, шаткость при ходьбе, нарушения равновесия в позе Ромберга при характерном широком расставлении ног, замедленная, скандированная речь свидетельствуют о заинтересованности червя мозжечка.
Различные сочетания поражения ядер черепных нервов, двигательных, координаторных, чувствительных нарушений, различные варианты спонтанного нистагма с учетом их топического представительства лежат в основе клинической диагностики повреждений ствола мозга. КТ и, особенно, МРТ уточняют локализацию, характер и распространенность травматического субстрата.
КТ И МРТ ДИНАМИКАКТ-динамика
Ушибы мозга легкой степени
При исследовании ушибов мозга легкой степени после ЧМТ в сроки до 1—2 мес в большинстве случаев обнаруживается нормальная КТ картина либо желудочковая система и подоболочечные пространства слегка расширены (см. рис. 10—5, см. т. I, рис. 19—2). Умеренное увеличение желудочковой системы, конвекситальных и базальных подоболочеч-ных пространств после отечных ушибов встречаются главным образом у больных пожилого возраста, а также у страдающих хроническим алкоголизмом. Следует подчеркнуть, что отмечаемые в отдаленном периоде диффузные КТ изменения у ряда пострадавших были зарегистрированы еще в остром периоде ЧМТ в такой же, либо меньшей степени.
Ушибы мозга средней степени
При динамическом КТ-исследовании ушибов мозга средней степени в сроки от 3 до 5 сут на фоне постепенного снижения плотности очажков геморрагии (вначале исчезают более глубинные кровоизлияния, затем субпиальные и кортикальные) выявляется нарастание перифокального отека, который в отдельных наблюдениях трансформировался в долевой. Усиление отека мозга сопровождается увеличением деформации близлежащих отделов желудочковой системы и подоболочечных пространств, а также в некоторых случаях смещением срединных структур до 5 мм.
КТ-исследование в сроки 15—30 сут указывает на полное или почти полное исчезновение участков повышенной плотности (см. рис. 10—1, см. рис. 12—8, 12—10, см. т. Т, рис. 19—3) и обусловливаемого ими объемного эффекта (регресс последнего завершается к 14—20 сут после ЧМТ). Если очажки кровоизлияния второго типа могли рассасываться на 3— 5 сут, то субпиальные кровоизлияния часто исчезали на 10—15 сут после ЧМТ. Примерно в этот же период становились изоплотными небольшие солитарные внутримозговые кровоизлияния. Об их рассасывании мог косвенно свидетельствовать полный регресс объемного эффекта к 20—25 сут (см. т. I, рис. 19—4). Исчезновение геморрагического ушиба и реакции мозга на него порой могли задерживаться под влиянием различных возрастных и преморбидных факторов.
В зоне геморрагических ушибов, включая небольшие солитарные кровоизлияния, в сроки от 1,5 до 2 мес выявляются участки пониженной плотности, которые в большинстве случаев в дальнейшем исчезают. По мере рассасывания кровоизлияний, регресса перифокального отека желудочковая система и подоболочечные пространства расправляются, могут появляться признаки диффузной атрофии мозга легкой или средней степени. В отдельных случаях на месте ушибов мозга средней степени формируются стойкие очерченные гиподенсивные гомогенные зоны, величина которых значительно уступает первоначальному объему геморрагического ушиба, коррелируя с истинными размерами очага деструкции (рис. 9—22, см. рис. 9—17, 9—18).
Рис. 9—22. Тяжелая ЧМТ с очагами размозжения в базальных отделах лобных долей больше справа. КТ динамика. Верхний ряд; при поступлении. Множественные участки геморрагического пропитывания, окруженные выраженным перифокальным отеком, переходящим в долевой и достигающим боковые желудочки. Смещение срединных структур влево на 7мм. Признаки дислокационной гидроцефалии. Средний ряд: спустя 14 суток после ЧМТ. Патологическая зона стала более гомогенная, долевой отек уменьшился, расправилась охватывающая цистерна. Нижний ряд: спустя 28 суток после ЧМТ. Полная редислокация желудочковой системы. Гиподенсивные участки на месте бывшего очага размозжепия.
У большинства пострадавших, перенесших геморрагические ушибы, желудочковая система имеет нормальные размеры, ширина цистерн, борозд и щелей колеблется в пределах возрастной нормы. В зоне бывших геморрагических ушибов часто выявляются ограниченные участки пониженной плотности, сочетающиеся с легким расширением желудочковой системы и подоболочечных пространств. Иногда после геморрагических ушибов в отдаленном периоде ЧМТ, наряду с очаговыми КТ-признаками средней степени, выявляется умеренная или выраженная вентрикуломегалия. Она сочетается с расширением конвекситальных борозд и щелей, что подтверждает наличие диффузного атрофического процесса.
Ушибы мозга тяжелой степени
Уже в первые часы после ЧМТ вокруг обширных
очагов размозжения появляется перифокальный отек (см. рис. 25). Он может быстро превращаться в долевой и затем, нередко имея четкую тенденцию к генерализации, распространяется на соседние доли гомолатерального, а затем и противоположного полушария. В таких случаях отмечается резкое сдавление желудочковой системы. Нередко наблюдается значительная асимметрия в распространении отека, что приводит к увеличению смещения срединных структур. В конечном итоге, может развиться дислокационная гидроцефалия. Нарастание полушарного отека обусловливает боковое сдавление нижневисочной извилины и ствола на уровне тенториального отверстия.
При отеке обеих лобных долей наблюдается заполнение хиазмальных цистерн смешенными задними отделами прямых извилин, в результате чего эти цистерны первыми перестают визуализироваться. Диффузный отек мозга, распространяющийся на оба полушария, вызывает сдавление обоих желудочков и — при полном истощении резервных подоболочечных пространств — приводит к аксиальному вклинению ствола мозга на уровне тенториального и/или большого затылочного отверстий. Сочетание полушарного и генерализованного отека приводит к различным комбинациям бокового и аксиального вклинения с нарастанием деформации и сужения цистерн основания вплоть до полного их исчезновения.
При менее массивных очагах размозжения лобных долей повреждение мозга распространяется на кору и подкорковое белое вещество на глубину не
более 2—3 см и может сочетаться с разрывом мягких мозговых оболочек (на что указывают признаки оболочечных плоскостных кровоизлияний над очагом размозжения). Если при них перифокальный отек превращается в долевой или распространяется на обе лобные доли, то увеличение объемного эффекта может приводить к развитию дислокационного КТ-синдрома средней степени выраженности. Его особенностью является смещение кзади суженных передних рогов желудочков, смещение срединных структур (не превышающее в области прозрачной перегородки 5, иногда — 7 мм), умеренная или выраженная деформация цистерн основания мозга.
При очаговых размозжениях лобных долей (по данным КТ) на 3—4 сут после ЧМТ отмечается стабилизация или увеличение отека мозга с тенденцией к распространению на вещество височных и теменных долей с нарастанием объемного эффекта (дальнейшее сужение просвета желудочковой системы и подоболочечных пространств, увеличение смещения срединных структур).
В динамике очага размозжения нередко можно отмстить слияние отдельных его участков и превращение — в результате некроза лежащей между кровоизлияниями неповрежденной мозговой ткани—в более гомогенную массу, которая затем из гиперденсивной постепенно переходит в изоден-сивную фазу и, поэтому, перестает визуализироваться. Несмотря на это, объемное воздействие очага размозжения сохраняется или очень медленно регрессирует, указывая на существование в нем не рассосавшейся размозженной ткани и сгустков крови, ставших изоплотными по отношению к окружающему отечному мозгу. Рассасывание патологического субстрата чаще происходит к 30—40 сут после ЧМТ, о чем свидетельствует исчезновение объемного эффекта и отечной реакции мозга (см. рис. 9-22, 9-25).
При КТ-исследованиях через 1,5—3 мес после ЧМТ в очаге размозжения обнаруживаются остаточные явления в виде зоны пониженной плотности корково-подкорковой локализации. Границы гиподенсивной зоны нечеткие и постепенно переходят в окружающую нормальную мозговую ткань. Объемный эффект отсутствует, как и деформация желудочковой системы и подоболочечных пространств (см. рис. 25). В эти сроки обычно еще нет сращения мозгового вещества с оболочками и эпендимарной выстилкой желудочков. В одних случаях указанные КТ-измснения длительно сохраняются, в других — постепенно трансформируются в зоны неравномерного снижения плотности, в проекции которых начинают визуализироваться кольцевые или удлиненные структуры слабо повышенной плотности; образуются мелкие одиночные или множественные кисты (см. рис. 25). Появляются первые признаки сращения с оболочками мозга в виде умеренной деформации подо бол очечных пространств и прилежащих мозговых структур. На таком очаговом фоне может улавливаться тенденция к развитию диффузной атрофии мозга; она тем отчетливей, чем выраженной очаговые посттравматические изменения. Нередко очень быстро, особенно у оперированных больных формируются обширные дефекты мозговой ткани.
Очаговые посттравматические изменения средней степени на КТ проявляются понижением плотности в базалъных отделах лобной доли. Обычно отмечается также сращение коры с оболочками головного мозга, а при наличии костного дефекта — и с мягкими тканями. Очаговые изменения средней степени нередко сопровождаются развитием умеренного диффузного атрофического процесса.
Очаговые посттравматические КТ-изменения тяжелой степени при повреждениях лобных долей в одних случаях представляют кистозные внутри-мозговые полости с четкими округлыми краями; плотность их содержимого соответствует плотности ЦСЖ. Полости нередко сообщаются с желудочковой системой и/или субарахноидалъным пространством. В других случаях очаговые КТ-изменения тяжелой степени проявляются обширными зонами пониженной плотности без четких границ, в проекции которых на фоне грубой тяжистости, определяются кольцеобразные и вытянутые тени повышенной плотности, что отражает напичие грубых рубцово-спаечных и атрофических процессов. При очаговых изменениях тяжелой степени обычно выявляется выраженное расширение желудочковой системы, преобладавшее в месте связи с порэнце-фалической кистой — зоне рубцово-спаечных или кистозно-спаечный процессов. Порэнцефалические кисты сообщаются с передним рогом и/или телом бокового желудочка, вовлекая в патологический процесс головку хвостатого ядра, зрительный бугор, внутреннюю и наружную капсулы.
При очагах размозжения височной доли, по данным КТ в динамике, часто быстро развивается перифокальный отек со склонностью к полушарному распространению, что приводит к значительному смещению срединных структур, к дислокационной гидроцефалии и, в конечном итоге, к вклинению гиппокампа в охватывающую цистерну с се тампонированием и ущемлением ствола в тенториальном отверстии. При КТ в этих случаях часто отмечается появление повторных кровоизлиянии и их слияние между собой; количество и суммарная плошадъ геморрагии увеличивается. Вследствие некроза отделенные друг от друга участки мозговой ткани пропитываются кровью, очаги размозжения становятся более гомогенными и объем их возрастает. На этом фоне возникают повторные кровоизлияния на отдалении — как в очагах повреждений, так и в практически неизмененной мозговой ткани. По данным КТ, через 1—2 мес завершаются процессы рассасывания некротизированной ткани и излившейся крови в височной доле.
После хирургических вмешательств с удалением травматического субстрата на КТ через 1 — 1,5 мес определяются значительные дефекты мозговой ткани, заполненные ЦСЖ и нередко связанные с желудочковой системой.
При консервативном лечении на месте очага размозжения височной доли по мере рассасывания начинает определяться полость с четкими краями с содержимым вначале слегка пониженной плотности, затем к исходу второго месяца приближающаяся к плотности ЦСЖ (см. рис. 9—17).
При сочетании внутримозговых гематом и очагов размозжения (при консервативном лечении) в процессе их инволюции формируются кистозные полости и рубцовоспаечные уплотнения. Параллельно с этим в сроки 1—2 мес на КТ нередко проявляется и диффузная атрофия мозговой ткани.
МРТ-динамика
МРТ является чувствительным методом в выявлении контузионных очагов, особенно в подострой стадии. Они обычно характеризуются гетерогенно измененной интенсивностью сигнала на томограммах по Т1 и на томограммах по Т2 за счет наличия геморрагических участков (рис. 9—23, см. рис. 9-16, 12-11).
В зависимости от выраженности деструктивных изменений, отека мозга, а также количества излившейся крови выделяют три вида очагов ушиба мозга.
При ушибе мозга легкой степени на МР-томограммах выявляется участок патологического сигнала, отражающий ограниченную зону отека, который часто подвергается обратному развитию без остаточных структурных изменений.
Ушибы мозга средней степени на МРТ выявляются в виде очаговых изменений гетерогенной или гомогенной структуры, что определяется особенностями кровоизлияний в зоне ушиба и их давностью, отражая ситуацию геморрагического пропитывания мозговой ткани без грубой ее деструкции.
Рис. 9—23. Очаги ушиба средней степени в лобно-базальных отделах правой лобной доли. МР — томограммы, А, Б — по Т1, В, Г — по Т2.
Ушибы мозга тяжелой степени, содержащие мозговой детрит, излившуюся кровь и отечную жидкость, на МРТ гетерогенны. В динамике МРТ-исследований их структура становится более однородной. Объемный эффект патологического субстрата регрессирует медленнее, свидетельствуя, что в очаге ушиба еще имеются нерассосавшаяся размозженная ткань и сгустки крови. Исчезновение по данным МРТ объемного эффекта к 30—40 сут после ЧМТ указывает на рассасывание патологического субстрата и формирование на его месте кистозно-атрофических зон (см. рис. 12—13).
Лечение
Объем, интенсивность и длительность фармакотерапии и других слагаемых консервативного лечения определяются тяжестью ушиба мозга, выраженностью его отека, внутричерепной гипертензии, нарушений микроциркуляции и ликворотока, а также наличием осложнений ЧМТ, особенностями преморбидного состояния и возрастом пострадавших.
Лечебные воздействия при ушибах мозга легкой и средней степени включают следующие основные направления: 1) улучшение мозгового кровотока; 2) улучшение энергообеспечения мозга; 3) восстановление функции ГЭБ; 4) устранение патологических сдвигов водных секторов в полости черепа; 5) метаболическая терапия; 6) противовоспалительная терапия.
Восстановление церебральной микроциркуляции — важнейший фактор, определяющий эффективность прочих лечебных мероприятий. Основным приемом здесь является улучшение реологических свойств крови — повышение ее текучести, снижение агрегационной способности форменных элементов, что достигается внутривенными капельными вливаниями реополиглюкина, кавинтона, производных ксантина (эуфиллин, теоникол) под контролем гематокрита. Улучшение микроциркуляции способствует усилению энергообеспечения мозга и предотвращению его гипоксии. Это особенно важно для восстановления и поддержания функции клеточных структур, составляющих ГЭБ. Таким образом осуществляется неспецифический мембраностабилизирующий эффект. В свою очередь, стабилизация мембранных структур нормализует объемные соотношения внутриклеточных, межклеточных и внутрисосудистых водных секторов, что необходимо для коррекции внутричерепной гипертензии. В качестве энергетического субстрата используют глюкозу в виде поляризующей смеси. Наличие в ней инсулина способствует не только переносу глюкозы в клетки, но и ее утилизации по энергетически выгодному пентозному циклу. Введение глюкозы содействует угнетению глюконеогенсза, функционально защищая гипоталамо-гипофизар-но-надпочечниковую систему (уменьшение выброса кортикостероидов) и паренхиматозные органы (снижение уровня азотистых шлаков).
Тканевая гипоксия при легких и среднетяжелых ушибах мозга развивается лишь в случаях несвоевременного или неполноценного устранения дыхательных нарушений в ранние сроки после ЧМТ или при развитии пневмонии.
Специфическое влияние на функцию ГЭБ оказывают эуфиллин, папаверин, способствующие накоплению циклического аденозинм оно фосфата, стабилизирующего клеточные мембраны. Учитывая многофакторное влияние эуфиллина на мозговой кровоток, функции клеточных мембран, проходимость дыхательных путей, то есть на те процессы и структуры, которые являются особо уязвимыми при острой ЧМТ, применение данного препарата при любом виде повреждения мозга является оправданным. Устранение резких колебаний АД также способствует поддержанию функции ГЭБ (предотвращение вазогенного отека или циркуляторной гипоксии мозга). В связи с тем, что при ушибе мозга происходит механический «прорыв» ГЭБ в зоне повреждения, а нервная ткань является чужеродной для иммунокомпетентной системы, с развитием в ряде случаев реакции аутоиммунной агрессии, в лечебный комплекс целесообразно включать гипосенси-билизирующие препараты (димедрол, пипольфен, супрастин в инъекциях, тавегил, препараты кальция).
Своевременное и рациональное использование многих из выше перечисленных средств при нетяжелых ушибах мозга часто предотвращает или устраняет нарушения распределения воды в различных внутричерепных секторах. Если они все же развиваются, то речь обычно идет о внеклеточном скоплении жидкости или об умеренной внутренней гидроцефалии. При этом традиционная дегидратациониая терапия салуретиками, а в более тяжелых случаях — осмодиуретиками (маннитол, глицерин) дает быстрый эффект. Дегидратационная терапия требует контроля осмолярности плазмы крови (нормальные показатели — 285—310 мосмоль/л).
При наличии массивного субарахноидального кровоизлияния в лечебный комплекс включают гемостатическую антиферментную терапию: 5% раствор аминокапроновой кислоты, контрикал, трасилол, гордокс. Последние три препарата обладают более мощным антигидролазным действием, и их использование блокирует многие патологические реакции, обусловленные выходом ферментов и других биологически активных веществ из очагов разрушения мозга. Препараты вводят внутривенно по 25—30 тыс. ЕД 2—3 раза в сут. Используют также дицинон и аскорутин.
Если при ушибах мозга имеются раны на голове, субарахноидальное кровоизлияние, и, особенно, ликворея, возникают показания к противовоспалительной терапии, в том числе предупредительной.
В лечебно-восстановительный комплекс обычно включают метаболическую терапию (ноотропы, церебролизин), а также вазотропные препараты, улучшающие церебральную микроциркуляцию (кавинтон, циннаризин, сермион и др.).
При ушибах мозга легкой и средней степени широко используют анальгетики и седативные, снотворные и гипосенсибилитирующие препараты. Порой возникают показания к назначению противосудорожных средств (депакин, фенобарбитал, клоназепам, карбамазепин и др.).
Длительность стационарного лечения, разумеется, при неосложненном течении ушибов легкой степени до 10—14 сут, при ушибах средней степени до 14—21 сут.
При ушибах мозга тяжелой степени (размозжениях его вещества) консервативное лечение осуществляется под контролем мониторинга общемозговой, очаговой и стволовой симптоматики, деятельности сердечно-сосудистой и дыхательной систем, температуры тела, важнейших критериев состояния гомеостаза, данных ЭЭГ, УЗДГ, КТ и др, а при показаниях и прямого измерения внутричерепного давления.
Интенсивная терапия тяжелых повреждений головного мозга специально рассмотрена в главе 7. Здесь лишь кратко укажем основные группы рекомендуемых при этом препаратов.
1. Дегидратанты: а) салуретики (лазикс — 0,5—1 мг на 1 кг массы тела в сут. внутримышечно);
б) осмотические диуретики (маннитол — внутривенно капельно в разовой дозе 1 — 1,5 г на 1 кг массы тела); в) альбумин, 10% раствор (внутривеннокапелъно 0,2—0,3 г на 1кг массы тела в сут.).
Применение для борьбы с отеком мозга при тяжелых его ушибах кортикостероидных гормонов в настоящее время исключено из признанных стандартов лечения ЧМТ, хотя кооперативные исследования в этом направлении вновь продолжены.
2. Ингибиторы протеолиза: а) контрикал (гордокс, трасилол) — вводят внутривенно капельнона 300—500 мл 0,9% раствора хлорида натрия в дозе
до 100000-150000 ЕД в сут. (разовая доза 20000-30000 ЕД) в течение первых 3—5 сут.
3. Антиоксиданты: а) эмоксипин 1 % раствора внутривенно капельно на 200 мл 0,9% раствора хлориданатрия в дозе 10—15 мг на 1 кг массы тела в сутки в течение 10—12 сут.; б) альфа-токоферола ацетат — до 300—400 мг в сутки внутрь в течение 15 сут.
4. Антигипоксанты — активаторы электрон-транспортной системы митохондрий: а) цитохром С — внутривенно капельно в дозе 50—80 мг в сутки
на 200 мл 0,9% раствора хлорида натрия в течение 10—14 сут; б) рибоксин до 400 мг в сутки внутривенно капельно на 250—500 мл изотонического раствора хлорида натрия в течение 10 сут.
5. Средства, способствующие регулированию агрегатного состояния крови: а) антикоагулянты прямого действия — гепарин (внутримышечно или
подкожно до 20000—40000 ЕД в сутки в течение 3—5 дней), после отмены которого переходят на прием непрямых антикоагулянтов; б) стимулято
ры (компламин по 5—6 мл 15% раствора внутривенно капельно (медленно) на 100—200 мл 5% раствора глюкозы; амбен — внутривенно капельно на 200 мл изотонического раствора хлорида натрия в разовой дозе 50—100 мг); в) средства, обладающие дезагрегирующими свойствами (трентал внутривенно капельно в дозе 0,1—0,2 г в сут на 250—500 мл 0,9% раствора хлорида натрия, реополиглюкин внутривенно капелъно 400—500 мл 5—10 сут, реоглюман внутривенно капельно в течение 4—5 дней из расчета 10 мл на 1 кг массы тела в сутки); г) нативная плазма (100—150 мл в сутки).
6. Антипиретики — реопирин, аспирин, литические смеси и парацетамол, анальгин.
7. Вазоактивные препараты — эуфиллин, кавинтон, сермион.
8. Нормализаторы обмена нейромедиаторов и стимуляторы репаративных процессов: а) Л-ДОПА (наком, мадопар) — внутрь по схеме до 3 г в сутки; б) ноотропы (ноотропил, пирацетам) — внутрь в суточной дозе 2,4 г, либо внутримышечно и внутривенно до 10 г в сутки; в) глиатилин — внутрь в
суточной дозе 1,2 г, либо внутримышечно и внутривенно по 1 г; г) церобролизин — по 1—5 мл внутримышечно или внутривенно.
9. Витамины: витамин В1 (исходя из суточной потребности, равной для взрослого человека 2—3мг), витамин В6 (в суточной дозе 0,05—0,1 г) внут
римышечно 20—30 сут; витамин С (0,05—0,1 г 2—3 раза в сут парентерально 15—20 сут).
10. Средства, снижающие иммунную реактивность организма по отношению к антигенам нервной ткани: дипразин (по 0,025 г 2—3 раза в сут),
супрастин (по 0,02 г 2—3 раза в сут), димедрол (по 0,01 г 2—3 раза в сут), по показаниям — иммуно-модуляторы (декарис, тималин, Т-активин, пентаглобулин и др.).
11. Антиконвульсанты: депакин, фенобарбитал, карбамазепин и др.
Перенесшие ушибы мозга подлежат длительному диспансерному наблюдению и — по показаниям — восстановительному лечению. Наряду с методами лечебной физкультуры, физиотерапии и трудовой терапии применяют метаболические (ноотропил, глиатилин, пирацетам, аминалон, пири-дитол и др.), вазоактивные (кавинтон, сермион, циннаризин, теоникол и др.), витаминные (В1, В6, В12, С, Е и др.), общетонизирующие препараты и биогенные стимуляторы (алоэ, стекловидное тело, ФиБС, актовегин, солкосерил, когитум, апилак, жень-шень, семакс и др.).
С целью предупреждения эпилептических припадков после ушибов мозга, в случаях, когда риск их развития обоснован, назначают препараты, содержащие фенобарбитал (паглюферал-1, 2, 3, глюферал и др.). Под контролем ЭЭГ показан их длительный однократный прием на ночь.
При возникновении эпилептических припадков терапию подбирают индивидуально с учетом характера и частоты пароксизмов, их динамики, возраста, преморбида и общего состояния больного.
Используют различные лротивосудорожныс и седативные средства, а также транквилизаторов. В последние годы, наряду с барбитуратами, часто применяют карбамазепин, тегритол, финлепсин и вальпроаты (конвулекс, депакин), а также ламиктал и габопентин.
К базисной терапии относят сочетание ноотропных и вазотропных препаратов. Ее предпочтительно проводить 2-х месячными курсами с интервалами 1—2 мес на протяжении 1—2 лет с учетом, разумеется, динамики клинического состояния.
Для профилактики и лечения посттравматических и постоперационных спаечных процессов целесообразно дополнительно использовать средства, влияющие на тканевой обмен: аминокислоты (церебролизин, глютаминовая кислота и др.), биогенные стимуляторы (алоэ, стекловидное тело и др.), ферменты (лидаза, лекозим и др.). По показаниям в амбулаторных условиях осуществляют также лечение различных синдромов послеоперационного периода — общемозговых (внутричерепной гипертензии или гипотензии, цефалгического, вестибулярного, астенического, гипоталамического и др.) и очаговых (пирамидного, мозжечкового, подкоркового, афазии и др.). При головных болях, наряду с традиционными анальгетиками, применяют танакан. При головокружении эффективен бетасерк. При нарушениях психики к наблюдению и лечению больных обязательно привлекают психиатра. У лиц пожилого и старческого возраста, оперированных в связи с ЧМТ, целесообразно усиление противосклеротической терапии.
Ушибы легкой степени подлежат только консервативному лечению. При ушибах мозга средней степени, как правило, показаний к хирургическому лечению не возникает. Ушибы мозга тяжелой степени или размозжения представляют собой субстрат, который может быть предметом оперативного вмешательства. Однако обоснована и концепция расширения показаний к консервативному лечению тяжелых ушибов мозга. Часто собственные саногенные механизмы организма при адекватной медикаментозной поддержке, способны лучше, чем хирургическая агрессия, справиться с грубыми повреждениями мозгового вещества. Защитную роль играют также «амортизирующий» эффект неповрежденного вещества мозга, особенно при локализации ушиба на отдалении от стволовых структур, дренирование избыточной жидкости вместе с продуктами распада в желудочковую систему или субарахноидальные пространства. Очевидно, до определенных пределов консервативное лечение лучше способствует развертыванию саногенных механизмов и компенсаторных возможностей пострадавшего мозга, чем хирургическое вмешательство.
Хирургическая агрессия не избавляет от неизбежных морфологических последствий очаговых повреждений вещества мозга. Вместе с тем она нередко влечет за собой дополнительную травматизацию мозга, особенно при радикальном удалении очагов размозжения. Выдвинутый для обоснования этого постулат «удаление очага ушиба мозга в пределах здоровых тканей» ошибочен, свидетельствуя о механистическом перенесении общих хирургических принципов оперирования патологических процессов (воспалительных, опухолевых и иных) мягких тканей, костей, внутренних органов на травматические поражения центральной нервной системы. Разные органы и разная природа поражения требуют различных подходов.
Результаты лечения как ближайшие, так и отдаленные, очевидно, являются наиболее объективным критерием — что обоснованней при очагах размозжения головного мозга: расширение сферы их радикального удаления, либо расширение сферы консервативной терапии.
Ю.В. Зотов и соавторы, анализирующие свой большой опыт хирургии очагов размозжения, где у 42% пострадавших было осуществлено их радикальное удаление (т.е. не только зоны деструкции мозгового вещества, но и так называемой переходной зоны, ширина которой колеблется в пределах 0,5—4 см), сообщают следующие данные. В Российском нейрохирургическом Институте им. А.Л. Поленова с 1974 по 1993 гг. было прооперировано 964 пострадавших с очагами размозжения головного мозга. Компьютерно-томографическая характеристика их не приводится. Общая летальность составила 45%. У 55% оперированных отмечены, как пишут авторы, благоприятные результаты. «При анализе результатов в зависимости от объема удаленного очага размозжения выявлено, что летальность при удалении очага размозжения до 20 см3 составляет 36%.»
При изучении катемнеза оперированных пострадавших по параметру трудовой адаптации Ю.В. Зотовым с соавторами установлено, что стойкая утрата трудоспособности — инвалиды 1 и II групп — наблюдается у 33%, снижение трудоспособности — инвалиды III и «рабочей» II группы — у 25%, восстановление трудоспособности с работой в прежних условиях у 39%; 3% — являются пенсионерами, не нуждающимися в постороннем уходе.
По данным Э.И. Гайтура, анализирующего гораздо более скромный опыт (81 наблюдение) Института нейрохирургии им. Н.Н. Бурденко за 1987—1996 гг. по дифференцированному лечению верифицированных на КТ очагов размозжения мозга, получены следующие результаты. Оперировано 20 пострадавших; летальность составила 30%, грубая инвалидизация — 15%, умеренная инвалидизация — 20%, хорошее восстановление — 35%,
Консервативное лечение проведено 61 пострадавшему (если объем очага размозжения не превышал 30 мл при височной локализации и 50 мл при лобной), из них умерло 11%, грубая инвалидизация — 15%, умеренная инвалидизация — 18%, хорошее восстановление — 56%.
Институтом нейрохирургии им. Н.Н. Бурденкотого КТ-МРТ-мониторинга в сопряжении с комплексным клиническим анализом и изучением катамнеза разработаны и апробированы следующие показания для консервативного лечения ушибов головного мозга тяжелой степени: 1) пребывание пострадавшего в фазе субкомпенсации или умеренной клинической декомпенсации; 2) состояние сознания в пределах умеренного или глубокого оглушения; при этом допустимо углубление нарушений сознания на короткий срок до сопора (по шкале комы Глазго не менее 10 баллов); 3) отсутствие выраженных клинических признаков дислокации ствола; 4) объем очага размозжения по КТ или МРТ данным менее 30 см3 для височной локализации и менее 50 см3 для лобной локализации; 5) отсутствие выраженных КТ или МРТ признаков боковой (смещение срединных структур не больше 5—7 мм) и аксиальной (сохранность или незначительная деформация охватывающей цистерны) дислокации мозга.
Рис. 9—24. Пострадавший 49 лет. Тяжелая черепно-мозговая травма с формированием множественных очагов ушиба в правом полушарии. Состояние после декомпрессивной трепанации слева, произведенной по месту первичной госпитализации. КТ динамика. А, Б, В — исследование на 7 сутки после ЧМТ на фоне перехода из сопора в оглушение. А — стандартная KT-TOMorpaMN-ra. Очаг размозжения в правой височной доле и меньший по размерам в передних отделах лобной доли. Деформация и смещение правого крыла охватывающей цистерны. Б — трехмерная КТ-реконструкция показывает уровень и соотношение очагов ушиба с мягкими тканями головы и костями черепа. В — трехмерная КТ-реконструкция с выделением поверхности больших полушарий мозга дает представление о распространенности контузионных очагов на кору, сопутствующем локальном субарахноидальном кровоизлиянии и перифокальном отеке.
Показаниями для хирургического вмешательства при размозжениях мозга являются: 1) стойкое пребывание пострадавшего в фазе грубой клинической декомпенсации; 2) состояние сознания в пределах сопора или комы (по шкале комы Глазго ниже
10 баллов); 3) выраженные клинические признаки дислокации ствола; 4) объем очага размозжения по данным КТ или МРТ больше 30 см3 (при височной локализации) и больше 50 см3 (при лобной локализации) при гомогенности его структуры; 5) выраженные КТ или МРТ признаки боковой (смещение срединных структур свыше 7 мм) и аксиальной (грубая деформация охватывающей цистерны) дислокации мозга.
Следует помнить, что значительная часть пострадавших с тяжелыми ушибами мозга относятся к так называемой группе риска. Они требуют интенсивной терапии при клиническом наблюдении в динамике с повторными КТ или МРТ (рис. 9—24, 9—25).
Рис. 9—24 (продолжение). Г, Д, Е — спустя 26 сут после ЧМТ. Г — стандартная КТ, Д — трехмерная КТ-реконструкция, Е — трехмерное КТ-выделение больших полушарий. На фоне восстановления сознания определяется разрешение очагов размозжения с формированием гиподенсивных зон, выходящих на конвекситальную кору, регресс пер и фокального отека, рассасывание субарах ноидальн о го кровоизлияния, расправление ликворосодержащих пространств.
Рис. 9—25. Пострадавший 70 лет с тяжелой ЧМТ — падение на затылок, перелом чешуи затылочной кости, очаги размозжения в базальных отделах лобных долей, больше справа, по механизму противоудара. Консервативное лечение. КТ динамика.
А, Б, В, Г — 1-е сутки после ЧМТ выявляются очаги размозжения в базальных отделах лобных долей больше справа.Умеренное оглушение.
Рис. 9 25 (продолжение). Д, Е, Ж, 3 — 2-е сутки после ЧМТ — нарастание объема и плотности очагов раз.чозжения с развитием перифокального отека. Глубокое оглушение.
Рис. 9—25(Продолжение). И, К, Л, М — 4-е сутки после ЧМТ. Дальнейшее увеличение очагов размозжения в сторону конвекситальных отделов лобных долей с признаками дальнейших кровоизлияний и объемного воздействия на передние рога боковых желудочков. Глубокое оглушение.
Рис. 9-25 (продолжение). Н, О, ГТ, Р — 14-е сутки. Постепенное понижение плотности очагов размозжения начиная с периферических отделов при прежней выраженности долевого отека. Умеренное оглушение.
Рис. 9—25 (продолжение). С, Т, У, Ф — 31-е сутки после ЧМТ. На месте очагов размозжения обширные гиподенсивные зоны. Расправление желудочковой системы, визуализация субарахноидальных пространств. Значительное клиническое улучшение.
Рис. 9—25 (окончание). X, Ц, Ч, Ш — 11-й месяц после ЧМТ. Очаговый спаечно-атрофический процесс в зоне расположения бывших очагов размозжения в лобных долях. Клиническое выздоровление.
Разумеется, представленные показания для дифференцированного лечения ушибов головного мозга применяются с учетом индивидуальных особенностей пострадавшего, оставляя врачу возможность принимать — при необходимости — нестандартные решения.
Методика и техника операций при ушибах мозга описаны в главе 1.
ПРОГНОЗ И ИСХОДЫ
Прогноз при ушибе мозга легкой степени обычно благоприятный (при условии соблюдения пострадавшим рекомендованного ему режима и лечения).
При ушибе мозга средней степени часто удается добиться полного восстановления трудовой и социальной активности пострадавших. У ряда больных развиваются асептический лептоменингит и гидроцефалия, обусловливающие астенизацию, головные боли, негетососудистую дисфункцию, нарушения статики, координации и другую неврологическую симптоматику.
Летальные исходы при среднетяжелых ушибах мозга наблюдаются редко и обусловлены либо некупируемыми гнойно-воспалительными осложнениями, либо отягощенным преморбидом, особенно у пожилых и стариков.
При ушибе мозга тяжелой степени прогноз часто неблагоприятный. Смертность достигает 25—30%. Среди выживших значительна инвалидизация, ведущими причинами которой яиляются психические расстройства, эпилептические припадки, грубые двигательные и речевые нарушения. По данным G. Teasdale, различной степени инвалидизация спустя 1 год после тяжелой ЧМТ достигает 78%. При открытой ЧМТ нередко возникают гнойно-воспалительные осложнения (менингит, энцефалит, вентрикулит, абсцессы мозга), а также ликворея.
И все же у многих пострадавших с размозжением мозга, если не было коматозного состояния или длительность его не превышала 24 ч, при адекватной тактике лечения удается добиться хорошего восстановления.
При ушибах мозга тяжелой степени, при отсутствии отягчающих обстоятельств и осложнений, в течение 3—6 недель часто отмечается регресс внутричерепной гипертензии, менингеальных симптомов, а также очаговой неврологической симптоматики (кроме краниобазальной, если она характеризовалась острым и полным нарушением функций черепных нервов).
Когда ЧМТ обусловливает грубые нарушения психики, то значительная ее нормализация часто отмечается спустя 2—3 месяца.
В качестве примера возможности благоприятного исхода при консервативном лечении ушибов головного мозга тяжелой степени приведем катамнез больного П., 71 г.
Клинический диагноз: тяжелая черепно-мозговая травма: крупные очаги размозжения в лобных долях, больше справа; перелом чешуи с переходом на основание черепа; ушибленно-рваные раны в затылочной и подбородочной областях.
Динамика состояния его сознания и компьютерных томограмм в остром периоде ЧМТ представлены на рис. 24.
Спустя 10 мес и 7 сут после получения ЧМТ (падение на затылок 22 февраля 2000 г.) и 8 мес и 25 сут после выписки П. 16 января 2001 г. был обследован в Институте нейрохирургии.
Жалоб не предъявляет, отмечает восстановление до травматического уровня физических и интеллектуальных своих возможностей и жизненной активности.
Со слов жены, «муж такой же, как и был до падения, может быть стал чуть раздражительней, но всегда по поводу, да и раздражительность его вполне терпимая».
Соматически — в пределах возрастных изменений; выглядит моложе своих лет.
Неврологически: контактен, активен, речь без каких-либо отклонений. Перкуссия черепа безболезненна. Зрачки равны, реакция на свет живая. Движения глаз в полном объеме. Едва заметная относительная сглаженность носогубной складки слева. Слабо положительный хоботковый рефлекс, двусторонний рефлекс Маринеску-Радовичи. Нет парезов конечностей, какой-либо убедительной асимметрии мышечного тонуса, сухожильных и брюшных рефлексов. Координаторные пробы выполняет четко с обеих сторон, походка — без отклонений, устойчив в позе сенсибилизированного Ромберга, нет менингеальных симптомов. Пробу на бимануальную реципрокную координацию выполняет без нарушений.
Психиатрическое исследование. В остром периоде спустя 3 нед после ЧМТ отмечен выход из спутанного состояния сознания через корсаковский синдром в ясное. Через 1 мес после травмы в клинической картине выявлялись эмоционально-личностные нарушения, характерные для поражения лобных долей (облегченная самооценка, благодушие) и некоторое снижение памяти на текущие события. Длительность ретро-антероградной амнезии ~ 1 мес. Спустя 3 мес — восстановление психики. Через 10 мес после травмы полностью себя обслуживает, активно занимается физкультурой, в поведении упорядочен. Со слов жены, болной практически полностью восстановился до того уровня, каким был до травмы. Отмечает лишь эпизоды раздражительности (незначительной). В беседе адекватен. Интересуется своими результатами. Критичен к своему состоянию. Достаточно быстро справляется с предложенными заданиями и пробами.
Рис. 9—26. Фрагмент ЭЭГ пострадавшего 70 лет спустя почти 11 мес после тяжелой ЧМТ с формированием крупных очагов размозжения в лобных долях. Отведения: О — затылочные, Р — теменные, С — центральные, F — лобные, Fp — лобно-полюсные, Т — височные; четные —слева, нечетные — справа. Умеренные общие изменения ЭЭГ с признаками раздражения коры и базально-диэнцефальных образований мозга. Эпилептиформные потенциалы и медленные формы активности преобладают в лобноцентральных областях без типичной эпиразряднои генерализации.
Нейропсихологическое исследование. Общителен. Охотно участвует в исследовании. Задания выполняет быстро. На первый план выступает импульсивность при выполнении заданий. Объективное нейропсихологическое исследование выявляет: Праксис позы сохранен, в пробах на динамический праксис легкие трудности удержания моторной программы. Перенос позы несколько затруднен с обеих рук, вероятно снижение кинестетической чувствительности слева. Тактильный гнозис: локализации точки прикосновения сохранна, чувство Ферстера несколько снижено с обоих сторон. Зрительный гнозис: умеренная фрагментарность восприятия проявляется в различных заданиях. Слуховой гнозис: встречаются ошибки по типу переоценки единичных ритмов и недооценки серийных; инертность при воспроизведении ритмических структур по слуховому образцу (продлевает ритмическую структуру вдвое сохраняя ритмический рисунок). Слухоречевая память: Легкое сужение объема запоминания 6 слов со 2-го предъявления. Некоторые нарушения избирательности следов (замена слов близкими по смыслу). Некоторая инертность при воспроизведении 2-х предложений. Зрительно-пространственные функции: Зеркальные ошибки при повороте фигур, а также «на следах памяти» при запоминании 6 фигур и отсроченном воспроизведении фигуры Тейлора. Единичные ошибки при оценки времени по «слепым» часам. При исследовании мышления обнаруживается импульсивность в решении задач, а также элементы опоры на латентные признаки.
Таким образом, обнаруживаются некоторые трудности контроля, легкие расстройства в гностической сфере. Мягкая нейропсихологическая симптоматика свиде гель с твуе т о неко торой дисфункции лобных о т-делов, преимущественно справа.
Электроэнцефалография (рис. 9—26). 1. Альфа-ритм, частотой 9,5—10 в секунду регистрируется нерегулярно с попеременной дезорганизацией то в левом, то в правом полушарии, снижен по амплитуде, регионарные различия периодами сглажены. 2. Реакция активации коры на афферентные раздражения несколько ослаблена по сравнению с нормой. 3. Частые синусоидальные, повышенной амплитуды бета-колебания отмечаются по перелдним отделам коры в сочетании с острыми двухфазными потенциалами, негрубыми пик-волновыми комплексами, а также эпизодическими вспышками билатеральных тета- и дельта-волн в лобно-центральных областях. 4. На фоне 2-минутной гипервентиляции подчеркивается синхронизация заостренных бета-колебаний по передним отделам коры.
Заключение. 1. Выявляются умеренные общие изменения ЭЭГ с признаками раздражения коры и ба-зально-диэнцефальных образований мозга. 2. Отмечаются локальные нарушения биопотенциалов в виде преобладания эпилептиформных потенциалов и медленных форм активности в лобно-центральных областях без типичной эпи-разрядной генерализации КТ — см. рис. 25х, ц, ч, щ.
Резюме. Итак, у 70-летнего мужчины, получившего тяжелую ЧМТ с переломом затылочной кости и образованием крупных противоударных очагов размозжения в лобных долях, консервативная тактика лечения позволила, по данным 10-ти месячного катамнеза, достичь хорошего восстановления, соответствующего практическому выздоровлению. Надо отметить, с одной стороны, неизбежное формирование спаечно-атрофического процесса в зонах разрешившихся очагов размозжения, а с другой, — полную и устойчивую клиническую компенсацию с регрессом имевших место лобных нарушений психики.
Стало быть, посттравматические очаговые изменения средней степени не всегда являются препятствием для хорошей медицинской и социальной реабилитации пострадавших, даже пожилого возраста.
По данным Института нейрохирургии им. Н.Н. Бурденко, при очагах размозжения мозга хорошее восстановление отмечено у 47,4% оперированных и у 78,3% кооперированных пострадавших, умеренная инвалидизация у 9,6% и 6,5%, грубая инвалидизация у 2,4% и 6,5%, соответственно; умерли 40,6% оперированных и 8,7% неоперированных пострадавших. При сравнительной оценке результатов лечения, конечно, следует учитывать, что к хирургическому вмешательству прибегали у более тяжелого контингента пострадавших.
Близкие результаты получены в Украинском НИИ нейрохирургии им. А.П. Ромоданова. При очаговых повреждениях мозга хорошее восстановление наблюдалось у 54,8% оперированных пострадавших и у 81,2% неоперированных, умеренная инвалидизация — у 17,7% и 10,6%, грубая инвалидизация — у 8,1% и 4,7%, соответственно; умерли 19,4% оперированных и 3,5% неоперированных пострадавших.
Сравнительный анализ отдаленных результатов выявил значительно лучшую социальную адаптацию, более ранний и в большем количестве наблюдений возврат к прежней работе пациентов при консервативном лечении очаговых повреждений головного мозга.
Л.Б. Лихтерман, А.А. Потапов, СЮ. Касумова, Э.И. Гайтур
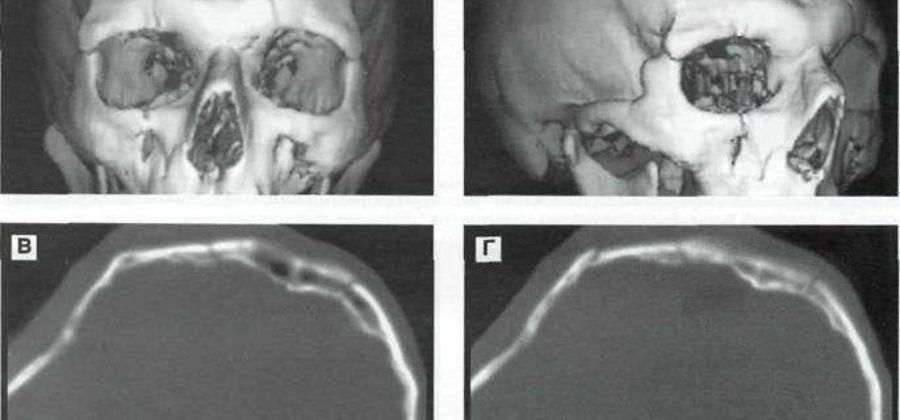

Отправляя сообщение, Вы разрешаете сбор и обработку персональных данных.
Политика конфиденциальности.